Впр функции excel: Функция ВПР — Служба поддержки Майкрософт
Содержание
Функция ВПР — Служба поддержки Майкрософт
Excel
Формулы и функции
Для работы со ссылками
Для работы со ссылками
Функция ВПР
Excel для Microsoft 365 Excel для Microsoft 365 для Mac Excel для Интернета Excel 2021 Excel 2021 for Mac Excel 2019 Excel 2019 для Mac Excel 2016 Excel 2016 для Mac Excel 2013 Excel 2010 Excel 2007 Excel для Mac 2011 Excel Starter 2010 Еще…Меньше
Совет: Попробуйте использовать новую функцию ПРОСМОТРX, улучшенную версию функции ВПР, которая работает в любом направлении и по умолчанию возвращает точные совпадения, что делает ее проще и удобнее в использовании, чем предшественницу.
Находите данные по строкам в таблице или диапазоне с помощью функции ВПР. Например, можно найти цену автомобильной детали по ее номеру или найти имя сотрудника по его идентификатору.
Самая простая функция ВПР означает следующее:
=ВПР(искомое значение; место для его поиска; номер столбца в диапазоне с возвращаемым значением; возврат приблизительного или точного совпадения — указывается как 1/ИСТИНА или 0/ЛОЖЬ).
Совет: Секрет функции ВПР состоит в организации данных таким образом, чтобы искомое значение (Фрукт) отображалось слева от возвращаемого значения, которое нужно найти (Количество).
Используйте функцию ВПР для поиска значения в таблице.
Синтаксис
ВПР(искомое_значение, таблица, номер_столбца, [интервальный_просмотр])
Например:
-
=ВПР(A2;A10:C20;2;ИСТИНА)
-
=ВПР(A2;’Сведения о клиенте’!A:F;3;ЛОЖЬ)
org/ListItem»>
=ВПР(«Иванов»;B2:E7;2;ЛОЖЬ)
|
|
|
|---|---|
|
|
Значение для поиска. Искомое значение должно находиться в первом столбце диапазона ячеек, указанного в аргументе таблица.
Например, если таблица охватывает диапазон ячеек B2:D7, искомое_значение должно находиться в столбце B.
|
|
|
Диапазон ячеек, в котором будет выполнен поиск искомого_значения и возвращаемого значения с помощью функции ВПР. Вы можете использовать именованный диапазон или таблицу, а также имена в аргументе вместо ссылок на ячейки.
Первый столбец в диапазоне ячеек должен содержать искомое_значение. Диапазон ячеек также должен содержать возвращаемое значение, которое нужно найти.
Узнайте, как выбирать диапазоны на листе .
|
|
|
Номер столбца (начиная с 1 для крайнего левого столбца таблицы), содержащий возвращаемое значение.
|
|
|
Логическое значение, определяющее, какое совпадение должна найти функция ВПР, — приблизительное или точное.
|
Начало работы
Для построения синтаксиса функции ВПР вам потребуется следующая информация:
-
Значение, которое вам нужно найти, то есть искомое значение.
-
Диапазон, в котором находится искомое значение. Помните, что для правильной работы функции ВПР искомое значение всегда должно находиться в первом столбце диапазона. Например, если искомое значение находится в ячейке C2, диапазон должен начинаться с C.
-
При желании вы можете указать слово ИСТИНА, если вам достаточно приблизительного совпадения, или слово ЛОЖЬ, если вам требуется точное совпадение возвращаемого значения. Если вы ничего не указываете, по умолчанию всегда подразумевается вариант ИСТИНА, то есть приблизительное совпадение.
org/ListItem»>
Номер столбца в диапазоне, содержащий возвращаемое значение. Например, если в качестве диапазона вы указываете B2:D11, следует считать B первым столбцом, C — вторым и т. д.
Теперь объедините все перечисленное выше аргументы следующим образом:
=ВПР(искомое значение; диапазон с искомым значением; номер столбца в диапазоне с возвращаемым значением; приблизительное совпадение (ИСТИНА) или точное совпадение (ЛОЖЬ)).
Примеры
Вот несколько примеров использования функции ВПР.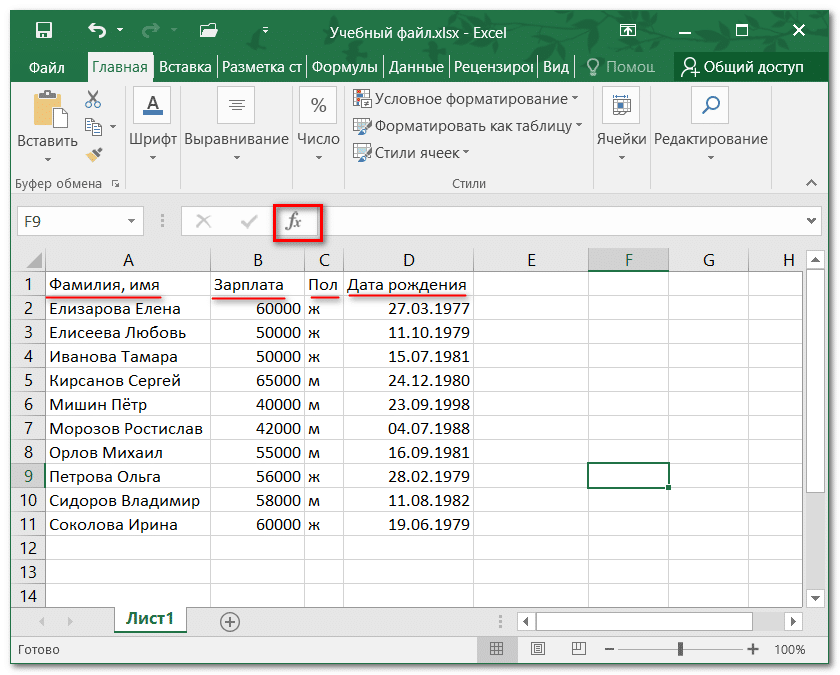
Пример 1
Пример 2
Пример 3
Пример 4
Пример 5
С помощью функции ВПР вы можете объединить несколько таблиц в одну, если одна из таблиц содержит поля, общие для всех остальных. Это может быть особенно удобно, если вам нужно поделиться книгой с пользователями более старых версий Excel, которые не поддерживают функции данных с несколькими таблицами в качестве источников данных. Благодаря объединению источников в одну таблицу и изменению источника функции данных на новую таблицу, функцию данных можно использовать в более старых версиях Excel (при условии, что функция данных поддерживается в более старой версии).
|
Здесь столбцы A–F и H содержат значения или формулы, которые используют значения только на этом листе, а в остальных столбцах используется функция ВПР и значения столбца А (код клиента) и столбца B (адвокат) для получения данных из других таблиц.
|
-
Скопируйте таблицу с общими полями на новый лист и присвойте имя.
-
Щелкните Данные > Работа с данными > Отношения, чтобы открыть диалоговое окно «Управление отношениями».
-
Для каждого отношения в списке обратите внимание на следующее.
-
Поле, которое связывает таблицы (указано в скобках в диалоговом окне). Это искомое_значение для вашей формулы ВПР.

-
Имя связанной таблицы подстановки. Это таблица в вашей формуле ВПР.
-
Поле (столбец) в связанной таблице подстановки, содержащее данные, которые вам нужны в новом столбце. Эта информация не отображается в диалоговом окне «Управление отношениями». Чтобы увидеть, какое поле нужно получить, посмотрите на связанную таблицу подстановки. Обратите внимание на номер столбца (A=1) — это номер_столбца в вашей формуле.
-
-
Чтобы добавить поле в новую таблицу, введите формулу ВПР в первом пустом столбце, используя сведения, собранные на шаге 3.

В нашем примере столбец G использует адвоката (искомое_значение) для получения данных ставки из четвертого столбца (номер_столбца = 4) из таблицы листа «Адвокаты», тблАдвокаты (таблица), с помощью формулы =ВПР([@Адвокат];тбл_Адвокаты;4;ЛОЖЬ).
Формула также может использовать ссылку на ячейку и ссылку на диапазон. В нашем примере это =ВПР(A2;’Адвокаты’!A:D;4;ЛОЖЬ).
-
Продолжайте добавлять поля, пока не получите все необходимые поля. Если вы хотите подготовить книгу, содержащую функции данных, которые используют несколько таблиц, измените источник данных для функции данных на новую таблицу.
|
|
|
|---|---|
|
Неправильное возвращаемое значение
|
Если аргумент интервальный_просмотр имеет значение ИСТИНА или не указан, первый столбец должны быть отсортирован по алфавиту или по номерам.
|
|
#Н/Д в ячейке
|
Дополнительные сведения об устранении ошибок #Н/Д в функции ВПР см. в статье Исправление ошибки #Н/Д в функции ВПР.
|
|
#ССЫЛКА! в ячейке
|
Если значение аргумента номер_столбца больше, чем число столбцов в таблице, появится значение ошибки #ССЫЛКА!.
Дополнительные сведения об устранении ошибок #ССЫЛКА! в функции ВПР см. в статье Исправление ошибки #ССЫЛКА!.
|
|
#ЗНАЧ! в ячейке
|
Если значение аргумента таблица меньше 1, появится значение ошибки #ЗНАЧ!.
Дополнительные сведения об устранении ошибок #ЗНАЧ! в функции ВПР см.
|
|
#ИМЯ? в ячейке
|
Значение ошибки #ИМЯ? чаще всего появляется, если в формуле пропущены кавычки. Во время поиска имени сотрудника убедитесь, что имя в формуле взято в кавычки. Например, в функции =ВПР(«Иванов»;B2:E7;2;ЛОЖЬ) имя необходимо указать в формате «Иванов» и никак иначе.
Дополнительные сведения см. в статье Исправление ошибки #ИМЯ?.
|
|
Ошибки #ПЕРЕНОС! в ячейке
|
Эта конкретная ошибка #ПЕРЕНОС! обычно означает, что формула использует неявное пересечение для искомого значения и применяет весь столбец в качестве ссылки. Например, =ВПР(A:A;A:C;2;ЛОЖЬ). Вы можете устранить эту проблему, привязав ссылку подстановки с помощью оператора @, например: =ВПР(@A:A;A:C;2;ЛОЖЬ).
|
|
|
|
|---|---|
|
Используйте абсолютные ссылки в аргументе интервальный_просмотр
|
Использование абсолютных ссылок позволяет заполнить формулу так, чтобы она всегда отображала один и тот же диапазон точных подстановок.
Узнайте, как использовать абсолютные ссылки на ячейки.
|
|
Не сохраняйте числовые значения или значения дат как текст.
|
При поиске числовых значений или значений дат убедитесь, что данные в первом столбце аргумента таблица не являются текстовыми значениями. Иначе функция ВПР может вернуть неправильное или непредвиденное значение.
|
|
Сортируйте первый столбец
|
Если для аргумента интервальный_просмотр указано значение ИСТИНА, прежде чем использовать функцию ВПР, отсортируйте первый столбец таблицы.
|
|
Используйте подстановочные знаки
|
Если значение аргумента интервальный_просмотр — ЛОЖЬ, а аргумент искомое_значение представляет собой текст, то в аргументе искомое_значение допускается использование подстановочных знаков: вопросительного знака (?) и звездочки (*).
Например, с помощью функции =ВПР(«Ивано?»;B2:E7;2;ЛОЖЬ) будет выполнен поиск всех случаев употребления Иванов с последней буквой, которая может меняться.
|
|
Убедитесь, что данные не содержат ошибочных символов.
|
При поиске текстовых значений в первом столбце убедитесь, что данные в нем не содержат начальных или конечных пробелов, недопустимых прямых (‘ или «) и изогнутых (‘ или “) кавычек либо непечатаемых символов. В этих случаях функция ВПР может возвращать непредвиденное значение.
Для получения точных результатов попробуйте воспользоваться функциями ПЕЧСИМВ или СЖПРОБЕЛЫ.
|
Дополнительные сведения
Вы всегда можете задать вопрос специалисту Excel Tech Community или попросить помощи в сообществе Answers community.
См. также
Функция ПРОСМОТРX
Видео: когда и как использовать ВПР
Краткий справочник: функция ВПР
Исправление ошибки #Н/Д в функции ВПР
Поиск значений с помощью функций ВПР, ИНДЕКС и ПОИСКПОЗ
Функция ГПР
Функция ВПР в Excel для чайников и не только
Функция ВПР в Excel позволяет данные из одной таблицы переставить в соответствующие ячейки второй.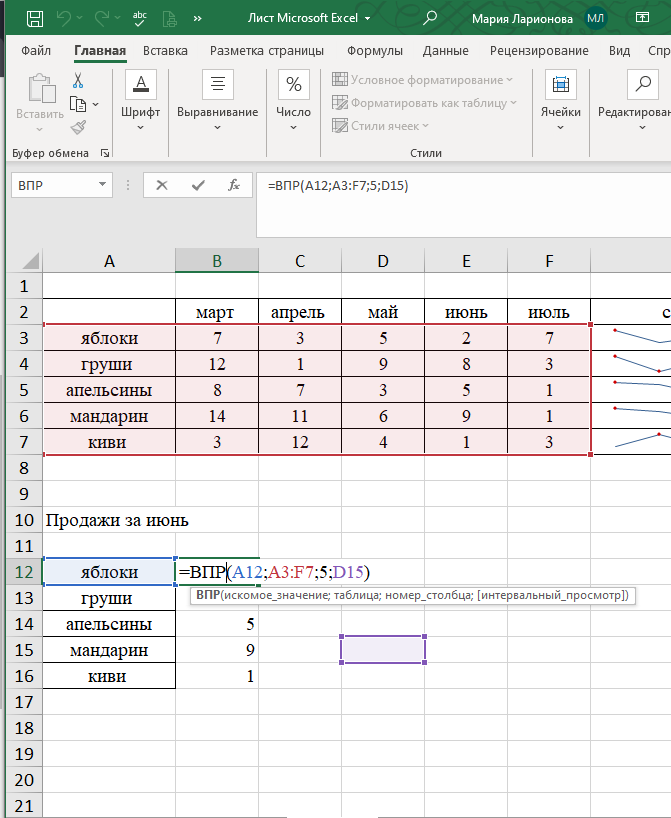 Ее английское наименование – VLOOKUP.
Ее английское наименование – VLOOKUP.
Очень удобная и часто используемая. Т.к. сопоставить вручную диапазоны с десятками тысяч наименований проблематично.
Как пользоваться функцией ВПР в Excel
Допустим, на склад предприятия по производству тары и упаковки поступили материалы в определенном количестве.
Стоимость материалов – в прайс-листе. Это отдельная таблица.
Необходимо узнать стоимость материалов, поступивших на склад. Для этого нужно подставит цену из второй таблицы в первую. И посредством обычного умножения мы найдем искомое.
Алгоритм действий:
- Приведем первую таблицу в нужный нам вид. Добавим столбцы «Цена» и «Стоимость/Сумма». Установим денежный формат для новых ячеек.
- Выделяем первую ячейку в столбце «Цена». В нашем примере – D2. Вызываем «Мастер функций» с помощью кнопки «fx» (в начале строки формул) или нажав комбинацию горячих клавиш SHIFT+F3. В категории «Ссылки и массивы» находим функцию ВПР и жмем ОК. Данную функцию можно вызвать перейдя по закладке «Формулы» и выбрать из выпадающего списка «Ссылки и массивы».

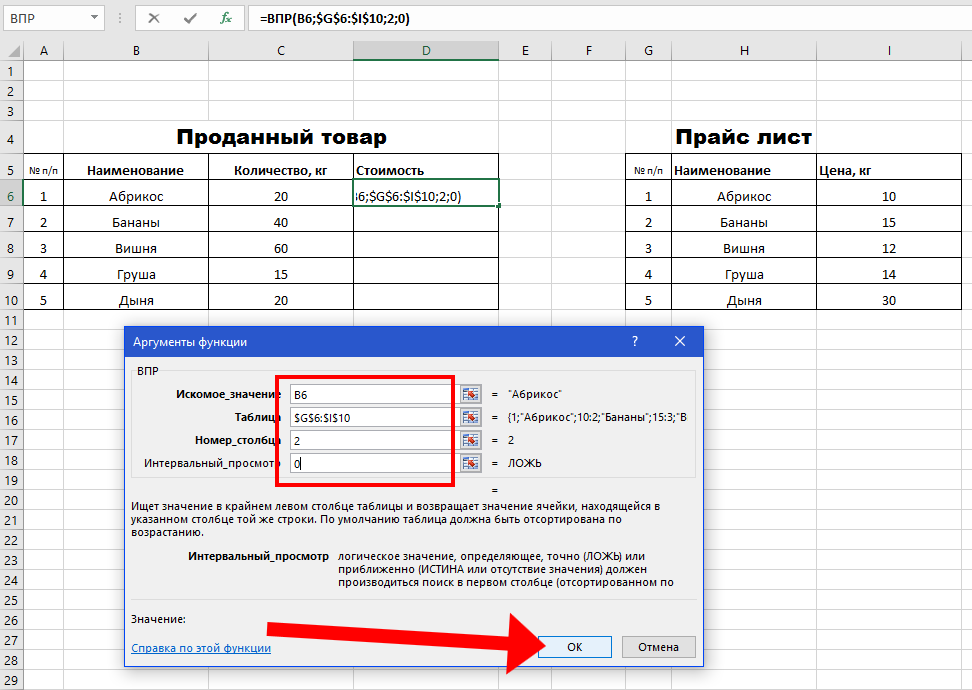
- Откроется окно с аргументами функции. В поле «Искомое значение» — диапазон данных первого столбца из таблицы с количеством поступивших материалов. Это те значения, которые Excel должен найти во второй таблице.
- Следующий аргумент – «Таблица». Это наш прайс-лист. Ставим курсор в поле аргумента. Переходим на лист с ценами. Выделяем диапазон с наименованием материалов и ценами. Показываем, какие значения функция должна сопоставить.
- Чтобы Excel ссылался непосредственно на эти данные, ссылку нужно зафиксировать. Выделяем значение поля «Таблица» и нажимаем F4. Появляется значок $.
- В поле аргумента «Номер столбца» ставим цифру «2». Здесь находятся данные, которые нужно «подтянуть» в первую таблицу. «Интервальный просмотр» — ЛОЖЬ. Т.к. нам нужны точные, а не приблизительные значения.
Нажимаем ОК. А затем «размножаем» функцию по всему столбцу: цепляем мышью правый нижний угол и тянем вниз. Получаем необходимый результат.
Теперь найти стоимость материалов не составит труда: количество * цену.
Функция ВПР связала две таблицы. Если поменяется прайс, то и изменится стоимость поступивших на склад материалов (сегодня поступивших). Чтобы этого избежать, воспользуйтесь «Специальной вставкой».
- Выделяем столбец со вставленными ценами.
- Правая кнопка мыши – «Копировать».
- Не снимая выделения, правая кнопка мыши – «Специальная вставка».
- Поставить галочку напротив «Значения». ОК.
Формула в ячейках исчезнет. Останутся только значения.
Быстрое сравнение двух таблиц с помощью ВПР
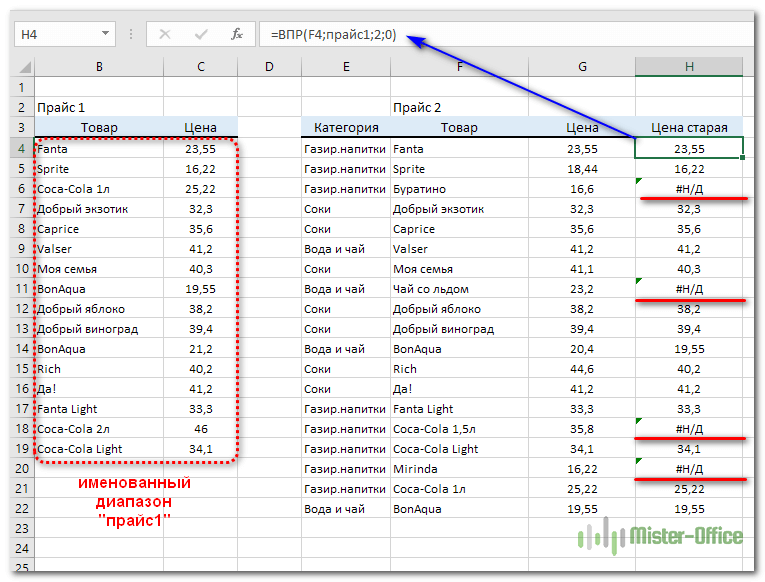
Функция помогает сопоставить значения в огромных таблицах. Допустим, поменялся прайс. Нам нужно сравнить старые цены с новыми ценами.
- В старом прайсе делаем столбец «Новая цена».
- Выделяем первую ячейку и выбираем функцию ВПР. Задаем аргументы (см. выше). Для нашего примера: . Это значит, что нужно взять наименование материала из диапазона А2:А15, посмотреть его в «Новом прайсе» в столбце А.
 Затем взять данные из второго столбца нового прайса (новую цену) и подставить их в ячейку С2.
Затем взять данные из второго столбца нового прайса (новую цену) и подставить их в ячейку С2.
Данные, представленные таким образом, можно сопоставлять. Находить численную и процентную разницу.
Функция ВПР в Excel с несколькими условиями
До сих пор мы предлагали для анализа только одно условие – наименование материала. На практике же нередко требуется сравнить несколько диапазонов с данными и выбрать значение по 2, 3-м и т.д. критериям.
Таблица для примера:
Предположим, нам нужно найти, по какой цене привезли гофрированный картон от ОАО «Восток». Нужно задать два условия для поиска по наименованию материала и по поставщику.
Дело осложняется тем, что от одного поставщика поступает несколько наименований.
- Добавляем в таблицу крайний левый столбец (важно!), объединив «Поставщиков» и «Материалы».
- Таким же образом объединяем искомые критерии запроса:
- Теперь ставим курсор в нужном месте и задаем аргументы для функции: .
 Excel находит нужную цену.
Excel находит нужную цену.
Рассмотрим формулу детально:
- Что ищем.
- Где ищем.
- Какие данные берем.
Функция ВПР и выпадающий список
Допустим, какие-то данные у нас сделаны в виде раскрывающегося списка. В нашем примере – «Материалы». Необходимо настроить функцию так, чтобы при выборе наименования появлялась цена.
Сначала сделаем раскрывающийся список:
- Ставим курсор в ячейку Е8, где и будет этот список.
- Заходим на вкладку «Данные». Меню «Проверка данных».
- Выбираем тип данных – «Список». Источник – диапазон с наименованиями материалов.
- Когда нажмем ОК – сформируется выпадающий список.
Теперь нужно сделать так, чтобы при выборе определенного материала в графе цена появлялась соответствующая цифра. Ставим курсор в ячейку Е9 (где должна будет появляться цена).
- Открываем «Мастер функций» и выбираем ВПР.
- Первый аргумент – «Искомое значение» — ячейка с выпадающим списком.
 Таблица – диапазон с названиями материалов и ценами. Столбец, соответственно, 2. Функция приобрела следующий вид: .
Таблица – диапазон с названиями материалов и ценами. Столбец, соответственно, 2. Функция приобрела следующий вид: . - Нажимаем ВВОД и наслаждаемся результатом.
Изменяем материал – меняется цена:
Скачать пример функции ВПР в Excel
Так работает раскрывающийся список в Excel с функцией ВПР. Все происходит автоматически. В течение нескольких секунд. Все работает быстро и качественно. Нужно только разобраться с этой функцией.
Функция ВПР (VLOOKUP) в Excel: пошаговая инструкция с примерами
В табличном редакторе Microsoft Excel множество различных формул и функций. Они позволяют сэкономить время и избежать ошибок – достаточно правильно написать формулу и подставить нужные значения.
В этой статье мы рассмотрим функцию ВПР (или VLOOKUP, что означает «вертикальный просмотр»). Функция ВПР помогает работать с данными из двух таблиц и подтягивать значения из одной в другую. Использовать ее удобно, когда нужно посчитать выручку или прикинуть бюджет, если в одной таблице указан прайс-лист, а в другой количество проданного товара.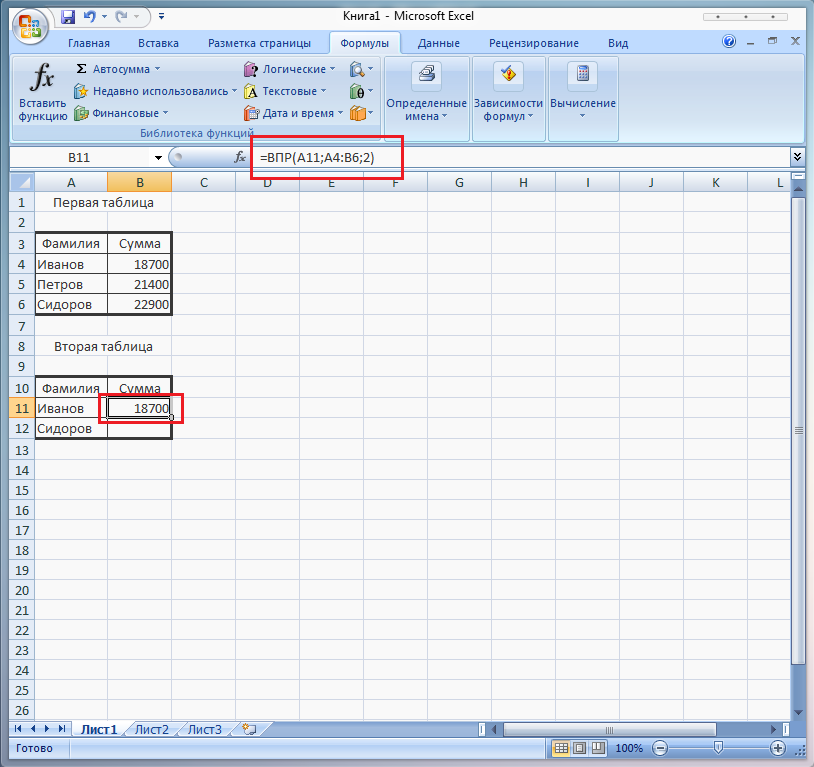
Допустим, есть таблица с количеством проданного товара и таблица с ценами на эти товары
Необходимо к каждому товару из таблицы слева добавить цену из прайса справа.
Как создать функцию ВПР в Excel
Необходимая последовательность значений в функции называется синтаксис. Обычно функция начинается с символа равенства «=», затем идет название функции и аргументы в скобках.
Записываем формулу в столбик цены (С2). Это можно сделать двумя способами:
-
Выделить ячейку и вписать функцию.
-
Выделить ячейку → нажать на Fx (Shift +F3) → выбрать категорию «Ссылки и массивы» → выбрать функцию ВПР → нажать «ОК».
После этого открывается окно, где можно заполнить ячейки аргументов формулы.
Синтаксис функции ВПР выглядит так:
=ВПР(искомое значение;таблица;номер столбца;интервальный просмотр)
В нашем случае получится такая формула:
=ВПР(A2;$G$2:$H$11;2;0)
Аргументы функции ВПР
Сейчас разберемся что и куда писать.
Со знаком равенства «=» и названием «ВПР» все понятно. Поговорим об аргументах. Они записываются в скобках через точку с запятой или заполняются в ячейки в окне функции. Формула ВПР имеет 4 аргумента: искомое значение, таблица, номер столбца и интервальный просмотр.
Искомое значение – это название ячейки, из которой мы будем «подтягивать» данные. Формула ВПР ищет полное или частичное совпадение в другой таблице, из которой берет информацию.
В нашем случае выбираем ячейку «A2», в ней находится наименование товара. ВПР возьмет это название и будет искать аналогичную ячейку во второй таблице с прайсом.
=ВПР(A2;
Таблица – это диапазон ячеек, из которых мы будем «подтягивать» данные для искомого значения. В этом аргументе используем абсолютные ссылки. Это значит, что в формуле таблица будет выглядеть как «$G$2:$H$11» вместо «G2:h21». Знаки «$» можно поставить вручную, а можно выделить «G2:h21» внутри формулы и нажать F4. Если этого не сделать, таблица не зафиксируется в формуле и изменится при копировании.
Если этого не сделать, таблица не зафиксируется в формуле и изменится при копировании.
В нашем случае – это таблица с прайсом. Формула будет искать в ней совпадение с ячейкой, которую указали в первом аргументе формулы – A2 (Кофе). Нажимаем F4 и делаем ссылку абсолютной.
=ВПР(A2;$G$2:$H$11
Номер столбца – это столбец таблицы, из которой нужно взять данные. Именно из него мы будем «подтягивать» результат.
-
Формула сканирует таблицу по вертикали.
-
Находит в самом левом столбце совпадение с искомым значением.
-
Смотрит в столбец напротив, очередность которого мы указываем в этом аргументе.
-
Передает данные в ячейку с формулой.
В нашем случае – это столбец с ценой продуктов в прайсе. Формула ищет искомое значение ячейки A2 (Кофе) в первом столбце прайса и «подтягивает» данные из второго столбца (потому что мы указали цифру 2) в ячейку с формулой.
=ВПР(A2;$G$2:$H$11;2
Интервальный просмотр – это параметр, который может принимать 2 значения: «истина» или «ложь». Истина обозначается в формуле цифрой 1 и означает приблизительное совпадение с искомым значением. Ложь обозначается цифрой 0 и подразумевает точное совпадение. Приблизительный поиск и критерий «истина» обычно используют при работе с числами, а точный и «ложь» – в работе с наименованиями.
В нашем случае искомое значение – это текстовое наименование. Поэтому используем точный поиск – ставим цифру 0 и закрываем скобку.
=ВПР(A2;$G$2:$H$11;2;0)
Комьюнити теперь в Телеграм
Подпишитесь и будьте в курсе последних IT-новостей
Подписаться
Автозаполнение
В конце протягиваем формулу вниз до конца, в результате чего происходит автозаполнение.
Чтобы функция ВПР правильно сработала во время автозаполнения, искомое значение должно быть относительной ссылкой, а таблица – абсолютной.
-
В нашем случае искомое значение – A2. Это относительная ссылка на ячейку, потому что в ней нет знаков «$». Благодаря этому ссылка на искомое значение меняется относительно каждой строчки, когда происходит автозаполнение в другие ячейки: A2 → A3 → … → A11. Это удобно, когда необходимо повторить формулу на несколько строк, ведь ее не приходится писать заново.
-
Таблица зафиксирована абсолютной ссылкой «$G$2:$H$11». Это означает, что ссылки на ячейки не изменятся во время автозаполнения. Таким образом, расчет каждый раз будет корректным и опираться на таблицу.
ВПР и приблизительный интервальный просмотр
В предыдущем примере мы «подтягивали» значения из таблицы, используя точный интервальный просмотр. Он подходит для работы с наименованиями. Теперь разберем ситуацию, когда может понадобиться приблизительный интервальный просмотр.
Задача. В магазин привезли товар. Необходимо присвоить каждому товару размер партии, опираясь на его количество.
Товары такие же, как и в первом примере, но задача изменилась: нужно привязать формулу не к наименованию, а к количеству
Решение. Заполняем формулу ВПР в ячейке «Партия», как было показано в предыдущем примере.
Разница в том, что теперь искомое значение – число, а интервальный просмотр – истина, что означает приблизительный поиск. Получается вот такой результат:
Что произошло? Аргумент «интервальный просмотр» имеет значение 1. Это значит, что формула ВПР ищет в таблице ближайшее меньшее искомое значение.
В нашем случае количество товара «Кофе» – 380. ВПР берет это число в виде искомого значения, после чего ищет ближайшее меньшее в соседней таблице – число 300. В конце функция «подтягивает» данные из столбца напротив («Крупная»). Если количество товара «Кофе» = 340 – это «Крупная партия». Важно, чтобы крайний левый столбец таблицы, которая указана в формуле, был отсортирован по возрастанию. В противном случае ВПР не сработает.
Значения и данные во второй таблице отсортированы по убыванию – ВПР не работает
Итоги
-
Функция ВПР означает вертикальный просмотр. Она просматривает крайний левый столбец таблицы сверху вниз.
-
Синтаксис функции: =ВПР(искомое значение;таблица;номер столбца;интервальный просмотр).
-
Функцию можно вписать вручную или в специальном окне (Shift + F3).
-
Искомое значение – относительная ссылка, а таблица – абсолютная.
-
Интервальный просмотр может искать точное или приблизительное совпадение с искомым значением.
-
Приблизительный поиск и критерий «истина» обычно используют при работе с числами, а точный и «ложь» – в работе с наименованиями.
-
Порядок работы с функцией подходит для Гугл-таблиц.
Функция ВПР в Excel — TutorExcel.
 Ru
Ru
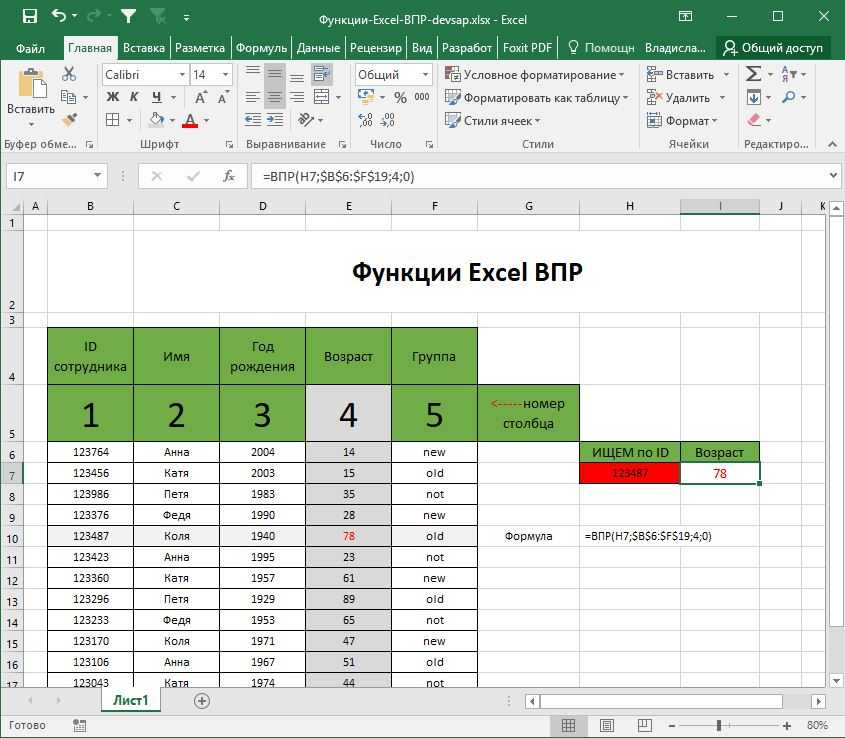
Изучим работу функции ВПР в Excel, которая связывает две таблицы и позволяет подтянуть данные из одной таблицы в другую.
Приветствую всех, дорогие читатели блога Tutorexcel.ru!
Мне кажется, что если подбирать ассоциацию к слову Excel, то с большим преимуществом победит вариант ВПР. Впрочем, уверен и в обратном, услышав слово ВПР сразу становится понятно, что речь идет про Excel.
Вот и мы сегодня поговорим про работу этой замечательной функции в Excel, которая позволяет быстро сопоставлять данные между несколькими таблицами, и на самом деле используется примерно в 100% всех файлов, наверное за исключением пустых книг 🙂
В общем давайте начинать и на примерах разберем пошаговую инструкцию по функции ВПР в Excel.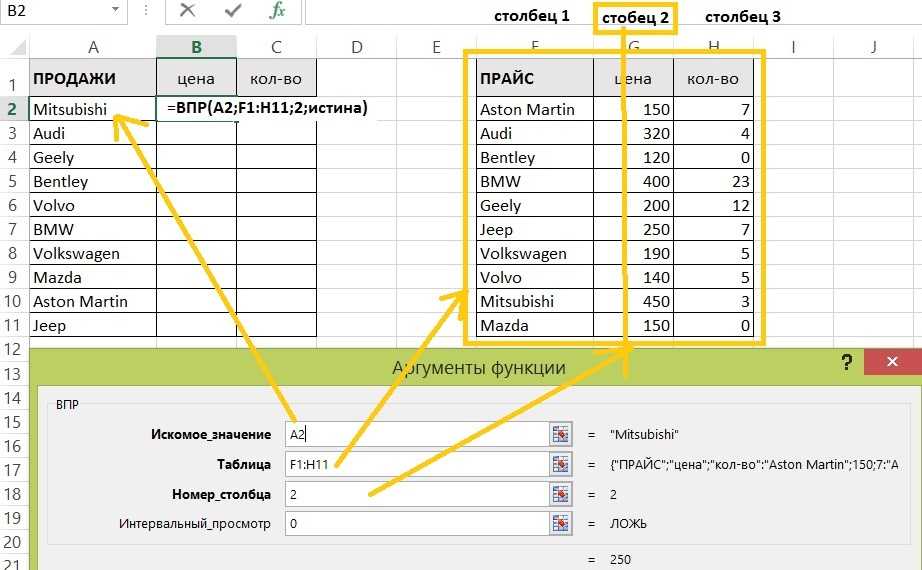
Функция ВПР в Excel. Синтаксис
Изучение любой функции начинаем с синтаксиса, функция ВПР (VLOOKUP в английской версии):
ВПР (искомое_значение; таблица; номер_столбца; [интервальный_просмотр])
Ищет значение в крайнем левом столбце таблицы и возвращает значение ячейки, находящейся в указанном столбце той же строки. По умолчанию таблица должна быть отсортирована по возрастанию.
Название ВПР получается из сокращения Вертикальный Просмотр, как раз по сути именно это функция и делает.
Познакомимся с каждым из аргументов по отдельности:
- Искомое значение (обязательный аргумент) — значение, которое должно быть найдено в первом столбце массива;
Обычно это числовое или текстовое значение. - Таблица (обязательный аргумент) — таблица с текстом, числами или логическими значениями, в которой производится поиск данных;
- Номер столбца (обязательный аргумент) — номер столбца в таблице, из которого нужно вернуть значение;
- Интервальный просмотр (необязательный аргумент) — логическое значение, определяющее, точно (ЛОЖЬ) или приближенно (ИСТИНА) должен производиться поиск в первом столбце.

Таким образом схему работы функции ВПР можно представить следующим образом — в таблице в первом столбце ищем искомое значение, находим строчку с этим значением и оставаясь в этой же строчке сдвигаемся вправо на номер столбца, значение из полученной ячейки и есть результат функции.
Со схемой познакомились, самое время перейти к практике.
Формула ВПР в Excel. Пример 1
Давайте рассмотрим пример, пусть у нас имеется таблица с прайс-листом товаров в магазине (артикул, наименование, цена в рублях, объем в литрах и вес в килограммах):
К нам в магазин приходит заказ и наша задача посчитать общую сумму заказа в деньгах:
Для того, чтобы посчитать сумму заказа нам не хватает цены за каждый из товаров, но эта информация как раз есть в исходной таблице которую мы и достанем с помощью функции ВПР.
Другими словами мы подтянем данные из первой таблицы во вторую и таким образом посчитаем общую сумма заказа.
Определимся с аргументами, в качестве искомого значения — артикул (G2), таблицы — исходная таблица с данными (A1:E11), номера столбца — третий (3), интервального просмотра — ЛОЖЬ (0, так как ищем точное соответствие), и записываем полученную формулу:
Визуально все сработало как надо, напротив каждого товара подтянулась нужная цена, теперь перемножаем количество на цены и получаем итоговый результат:
На первый взгляд все получилось достаточно просто, но здесь есть несколько подводных камней, давайте разберем основные из них.
Ошибки при работе с функцией ВПР в Excel
Не закрепление диапазона в таблице
При использовании ВПР в качестве как минимум 2 аргументов (исходного значения и таблицы) используются ссылки на ячейки или диапазоны. Поэтому крайне важно грамотно прописывать ссылки и при необходимости закреплять формулы, так как при протягивании формул ссылки могут сбиться и в результате мы можем получить ошибочный результат.
В нашем примере если мы забудем зафиксировать диапазон таблицы A1:E11, то при протягивании формулы он сначала превратится в A2:E12, затем в A3:E13 и т.д.
В итоге для одного из товаров мы получим ошибку, так как нужного артикула в смещенной таблице уже нет:
Поиск не по первому столбцу
При выборе аргумента таблицы очень важно, чтобы поиск происходил именно по первому столбцу таблицы. Бывают ситуации, что таблица содержит много столбцов, мы автоматически выделяем всю таблицу, хотя производить поиск хотим не по первому столбцу.
В нашем случае, к примеру, если мы хотим искать по наименованию (которые находятся в столбце B), то в качестве таблицы нужно выбирать диапазон B1:E11 (не A1:E11), так как именно по столбцу B будет делаться поиск и именно он является первым столбцом в таблице B1:E11.
Пропуск интервального просмотра
Интервальный просмотр необязательный аргумент функции ВПР, поэтому при записи формулы его формально можно не писать. Проблема в том, что если его не прописать, то по умолчанию он считается равным 1 (ИСТИНА), таким образом поиск идет не по точному, а по приближенному значению.
Проблема в том, что если его не прописать, то по умолчанию он считается равным 1 (ИСТИНА), таким образом поиск идет не по точному, а по приближенному значению.
Для поиска по приближенному значению необходимо, чтобы таблица была отсортирована по возрастанию, в ином случае возможна некорректная работа функции, про работу приближенного поиска расскажу в отдельной статье, так как в большинстве случаев нужен именно точный поиск.
В нашем случае пропуск параметра приводит к тому, что ВПР находит совершенно не то, что нужно, как раз из-за приближенного поиска:
Смена номера столбца
Аргумент номер столбца для функции очень часто прописывается как число в явном виде (например, 3, 4 или 7). Проблема может возникнуть тогда, когда в исходной таблице поменяется порядок столбцов. Например, мы решим добавить в таблицу новый столбец или наоборот, удалить лишний столбец, и то, что раньше было, к примеру, третьим столбцом может стать четвертым или вторым.
Если в наш пример добавить в середину таблицы новый столбец, то исходный третий столбец с ценой станет четвертым, а уже новый третий столбец станет пустым, поэтому формула ВПР вместо цены вернет пустые значения:
Идем дальше.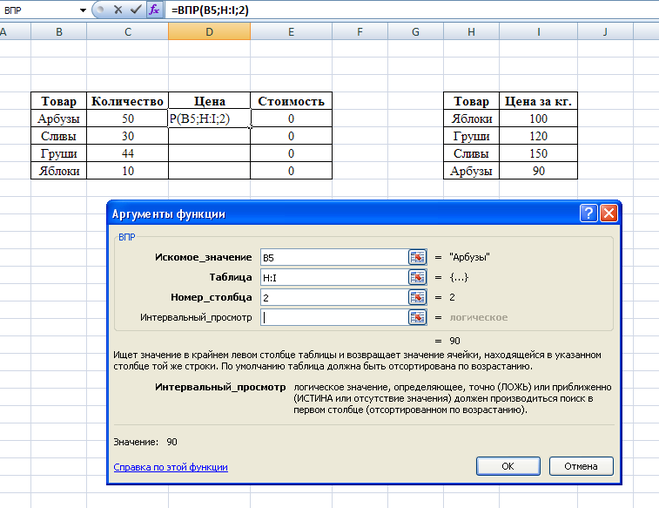
Функция ВПР в Excel. Пример 2
Для закрепления материала давайте рассмотрим еще один пример и сделаем сравнение двух таблиц посредством функции ВПР.
Немного модифицируем таблицу из предыдущего примера и рассмотрим 2 варианта таблицы (старый и новый прайс-листы), так как достаточно часто встречается задача сравнить одинаковые по структуре данные, которые могли быть видоизменены:
Так же как видим в правой таблице для усложнения перемешаны строчки с товарами (теперь они уже идут не по порядку), чтобы задача решалась не простым вычитанием, а все-таки с помощью более интересных инструментов 🙂
Давайте подтянем справа от новой цены старую, для этого прописываем функцию ВПР, в качестве аргумента искомого значения указываем название товара (D3), таблицы — левую часть исходной таблицы (A2:B12), номера столбца — второй (2), интервального просмотра — ЛОЖЬ (0) и не забываем закреплять диапазоны в случае необходимости, чтобы ссылки не сбились:
Старую цену подтянули, теперь осталось только сравнить полученные значения, в соседнем столбце прописываем разницу между столбцами, для наглядности ячейки отличные от нуля можно подсветить дополнительной заливкой для лучшей визуализации отклонения:
Резюмируем, с основными особенностями работы функции ВПР мы познакомились, надеюсь, что теперь пользоваться данной формулой вам будет еще проще и понятнее.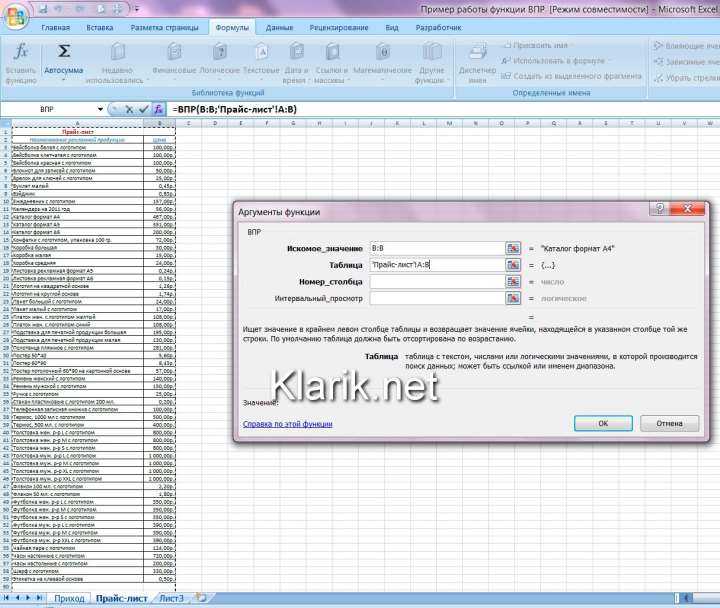
Скачать файл с примером.
Спасибо за внимание!
Если у вас остались вопросы, то обязательно делитесь ими в комментариях.
Удачи вам и до скорых встреч на страницах блога TutorExcel.Ru!
Поделиться с друзьями:
Поиск по сайту:
Формулы,Функции
Как работает впр в excel пошагово
Как работает впр в excel пошагово
Даже, если Вы не часто открываете Excel, будет очень полезно знать впр эксель и как пользоваться этой функцией. Статья рассказывает, как работает функция впр в excel для чайников. Здесь Вы найдете как работает впр в excel пошагово с примерами, их скриншотами и описанием.
Для более комфортного пользования функций ВПР будет полезным знать, как работают ссылки в Excel, и какие существуют правила закрепления ссылок.
Функция впр в excel для чайников
Функция ВПР – расшифровывается, как вертикальный просмотр. Это, казалось бы мало практичная деталь, позволяет разобраться в принципе работы функции ВПР.
Если Вы знаете принцип работы функции, то можно пролистать до следующего блока.
Представьте, что Вам нужно заполнить таблицу с ведомостью по зарплатам сотрудников конкретного отдела.
У Вас уже есть шаблон ведомости, в котором заполнены табельные номера и ФИО.
Осталось внести суммы зарплат и собрать подписи.
Шаблон зарплатной ведомости
Сведения о заработной плате находятся в другой таблице, например в общем реестре предприятия, где есть табельный номер и зарплата каждого сотрудника.
Без функции Вы бы искали каждый табельный номер в общем списке сверху вниз, потом переписывали или копировали бы з/п напротив нужного табельного в свою таблицу.
Заполнение таблицы вручную
Собственно, по такому же принципу и работает ВПР, делает просмотр сверху вниз (вертикально) до требуемого значения идентификатора и забирает значение напротив, как результат вычисления.
ВПР эксель как пользоваться
Функция ВПР находится в разделе функций ссылок и массивов.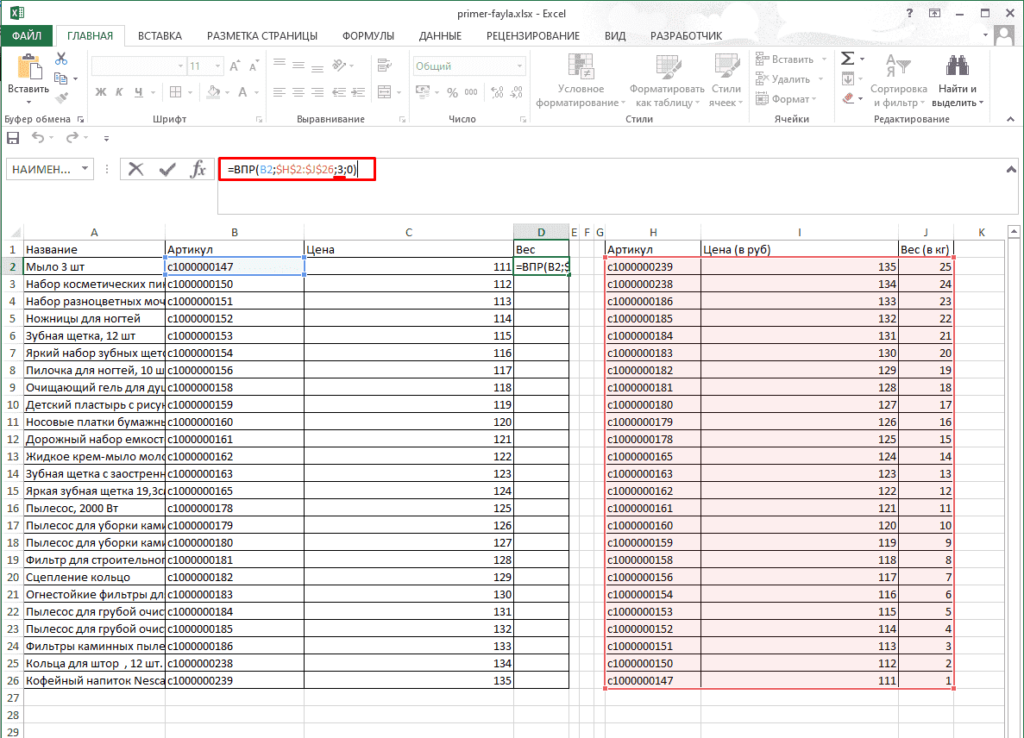
Как найти ВПР
Функцию ВПР обычно вставляют в ячейку, в которой будет итоговый результат, в нашем случае зарплата конкретного сотрудника в ведомости.
Функция впр в excel примеры: где писать функцию
Теперь нужно последовательно заполнить четыре аргумента функции ВПР.
Искомое значение – значение для поиска. Значение, которое вы хотите найти. Поиск этого значения будет в первом столбце диапазона ячеек, указанного в аргументе — Таблица.
В нашем примере с зарплатной ведомостью – это табельный номер первого сотрудника в ведомости. Поэтому мы в этом аргументе можем просто указать адрес ячейки табельного в таблице ведомости.
Функция впр в excel примеры: Искомое значение.
Таблица – диапазон ячеек, в котором будет выполнен поиск искомого значения и возвращаемого значения с помощью функции ВПР. Первый столбец в диапазоне ячеек должен содержать искомое значение. Диапазон ячеек также должен содержать возвращаемое значение, которое нужно найти.
Диапазон ячеек также должен содержать возвращаемое значение, которое нужно найти.
В нашем случае – это таблица общего реестра предприятия. При этом первым мы будем делать столбец, в котором функция будет искать табельный номер. Последний столбец не так важен, главное, чтобы в таблицу входил столбец, из которого мы будем забирать значение.
Если Ваша формула будет протягиваться, то обязательно закрепите диапазон таблицы используя клавишу F4.
Функция впр в excel примеры: Таблица
Номер столбца – номер столбца начиная с 1 для самого левого столбца Таблицы, содержащего возвращаемое значение.
В текущем примере у нас таблица начинается со столбца «Табельный номер» и заканчивается столбцом «Зарплата», поэтому номер столбца будет 2. Т.к. он второй в нашей таблице.
Функция впр в excel примеры: Номер столбца.
Интервальный просмотр – число 0 или 1.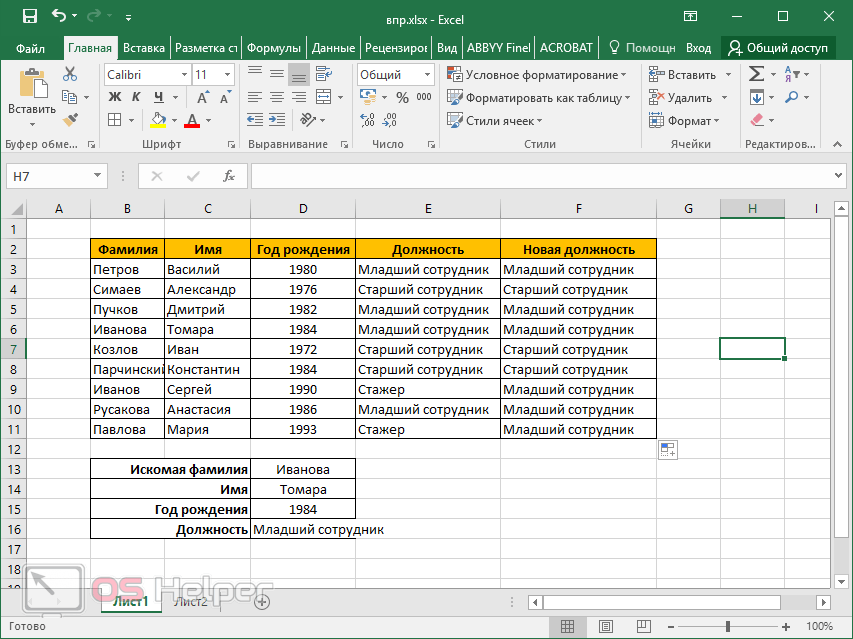
0 (Ложь [False]) Точное совпадение–осуществляет поиск точного значения в первом столбце(если не находит –#Н/Д [#N/A]).
1 (Истина [True]) Приближенное соответствие–если нет совпадения, то выдает max_значение <искомого, при этом выделенная таблица должна быть отсортирована по первому столбцу по возрастанию.
В примере с ведомостью нам нужно строгое соответствие табельного номера, как и в большинстве случаев на практике. Мы обязательно сделаем отдельную статью, про то, как правильно использовать 1 в этом аргументе.
А пока просто запомните, что здесь всегда ставим 0.
Функция впр в excel примеры: Интервальный просмотр.
Как работает функция впр в excel пример.
Работу функции ВПР в excel можно изобразить таким образом:
Как использовать функцию впр в excel примеры.
Самые частые ошибки функции ВПР в excel.
Обычно при работе с функцией ВПР допускают только 2 ошибки:
1. Формула ВПР работает, но когда протягиваешь её, то значения неправильные.
Формула ВПР работает, но когда протягиваешь её, то значения неправильные.
В этом случае нужно обязательно проверить правильно ли сделано закрепление ссылок. В первую очередь закреплена ли таблица.
2. Функция ВПР выдает значения, но проверка показывает, что они неправильные. Скорее всего 4ый аргумент функции ВПР не заполнен или равен 1 (что, по сути, одно и тоже). Проследите, чтобы четвертый аргумент был равен 0.
ВПР
Функция excel ВПР
Ещё у нас есть online курс Функции и форматирование, пройдя который Вы получите практические навыки в работе с самыми востребованными функциями Excel.
ВПР в Excel для облегчения работы с таблицами
Что это? Функция ВПР в Еxcel (или иначе VLOOKUP, то есть вертикальный просмотр) позволяет работать с двумя таблицами одновременно, оперируя их данными путем переноса значений из одной в другую.
Зачем нужна? К примеру, вам нужно оценить бюджет предстоящего маркетингового мероприятия, когда в одной таблице прайс-лист, а в другой – предполагаемое количество единиц разного мерча.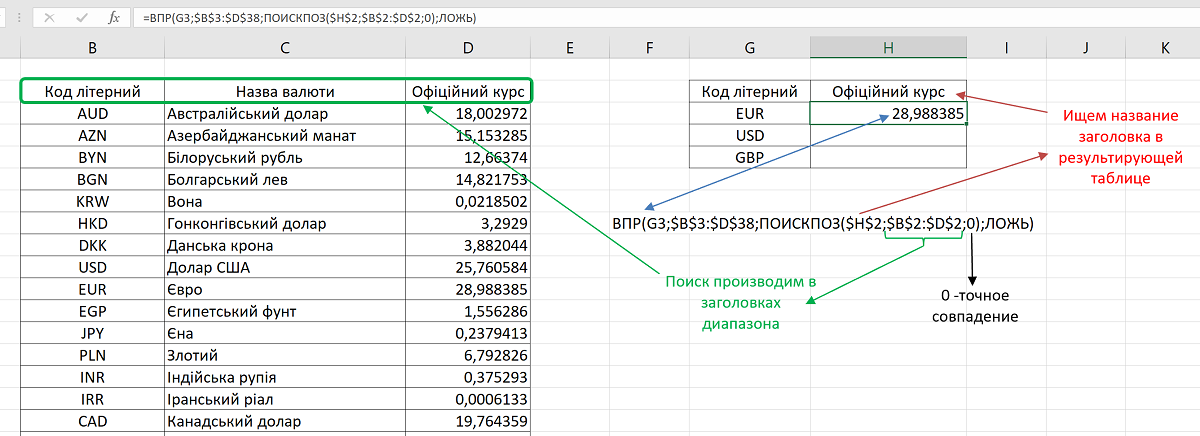 Как же в этом случае использовать ВПР в Еxcel?
Как же в этом случае использовать ВПР в Еxcel?
В статье рассказывается:
- Зачем нужна функция ВПР в Excel
- Пошаговая инструкция по работе с ВПР в Excel
- Поиск по нескольким критериям
- Быстрое сравнение двух таблиц с помощью ВПР в Excel
Пройди тест и узнай, какая сфера тебе подходит:
айти, дизайн или маркетинг.Бесплатно от Geekbrains
Зачем нужна функция ВПР в Excel
Допустим, вы занимаетесь продажей автомобилей. У вас есть две таблицы: в одной указаны характеристики и цены каждой модели, в другой находится список клиентов с контактами, которые желают приобрести ту или иную машину.
Перед вами стоит задача обзвонить всех потенциальных покупателей, чтобы сообщить окончательную стоимость выбранного ими автомобиля. Но прежде требуется сопоставить имеющиеся у вас данные путем переноса колонки с ценой в таблицу с данными клиентов.
Зачем нужна функция ВПР в Excel
Однако сделать это не так просто.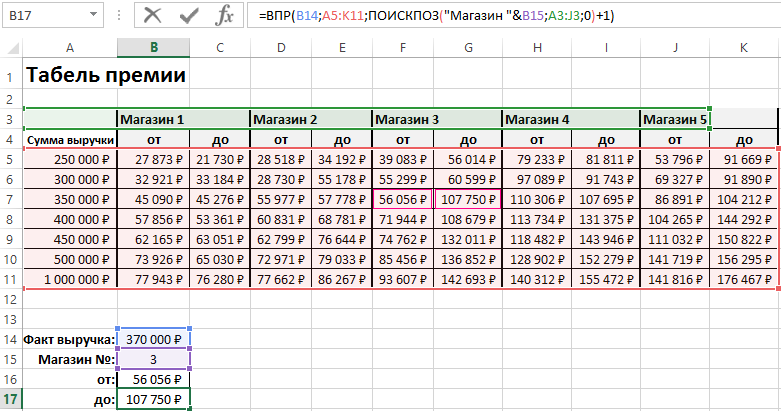 Нужного результата вы не достигнете, если просто скопируете и вставите столбец. А поиск и перенос цен вручную – долгая и кропотливая работа.
Нужного результата вы не достигнете, если просто скопируете и вставите столбец. А поиск и перенос цен вручную – долгая и кропотливая работа.
Как раз с помощью функции ВПР в Excel можно произвести сравнение двух таблиц и перенести стоимость забронированных автомобилей из каталога в клиентский список.
Следует знать, что пользоваться ВПР в Excel можно только при условии, что таблицы находятся в одном файле, но на разных листах.
Пошаговая инструкция по работе с ВПР в Excel
Итак, как работает ВПР в Excel? На самом деле принцип довольно прост: функция анализирует выбранный диапазон таблицы, двигаясь сверху вниз в поисках заданного значения. Как только идентификатор найден, ВПР копирует в другую таблицу данные из нужной колонки напротив него.
Ниже мы разберем, как происходит определение требуемых значений, а прямо сейчас предлагаем понятную инструкцию – как сделать ВПР в Excel на примере продажи автомобилей.
Шаг 1. Построение функции
Первым делом следует выделить ячейку, в которую формула скопирует искомое значение.
В нашем примере это цены на машины, которые забронировали клиенты. Поэтому во второй таблице требуется создать столбец, прописать его название: «Цена» и выделить в нем ячейку напротив первого покупателя.
Приступаем к построению функции. Сделать это можно двумя способами: во вкладке «Формулы» выбрать пункт «Вставить функцию» либо в строке ссылок нажать на значок «fx».
После этого откроется окно «Построитель формул», в котором, используя поиск, нужно найти ВПР, а затем нажать кнопку «Вставить функцию».
Далее появится поле для ввода аргументов, которое необходимо заполнить. А как это сделать смотрим ниже.
Шаг 2. Заполнение значений функции
Перед тем, как объяснить выбор аргументов, рассмотрим понятие каждого.
Искомое значение, то есть наименование ячейки, содержащей данные, одинаковые для обеих таблиц. Именно по ним функция ВПР будет искать нужные. В нашем случае искомое значение – это модель автомобиля. ВПР находит ее в каталоге, берет соответствующую ей цену и копирует в таблицу с клиентами.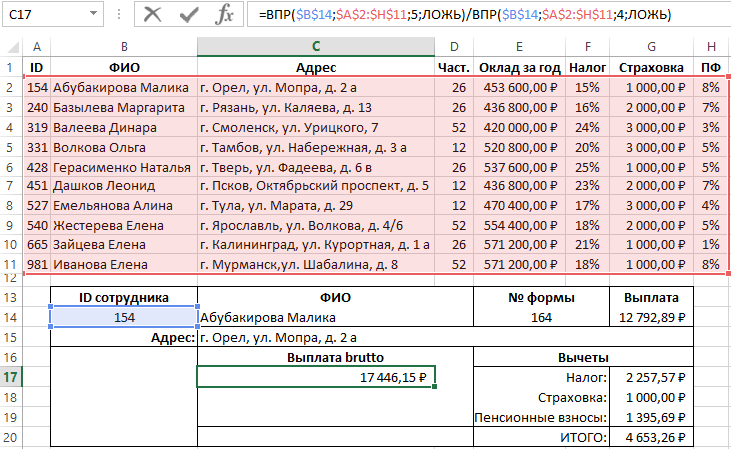
Заполнение значений функции
Как установить данный параметр?
- Курсор устанавливаем в поле «Искомое значение» в окне «Построитель формул».
- Выбираем ячейку А2, в которой содержится первое значение из столбца моделей автомобилей.
- Значение, которое мы указали, помимо построителя формул, дублируется в формуле строки ссылок, которая выглядит так: fx = ВПР (А2).
Таблица представлена диапазоном ячеек, из которого функция ВПР Excel выбирает данные для искомого значения. В него должны быть включены колонки с ним и теми данными, которые нужно подставлять в таблицу.
У нас это стоимость автомобилей. Соответственно, в область работы функции мы включаем столбцы «Модель», которые является искомым значением и «Цена», то есть то, что будет перенесено.
Обращаем внимание! Для корректной работы формулы диапазон должен начинаться с ячейки, с искомым значение, расположенной в первой колонке. В нашем примере это А2.
Последовательность действий при выборе диапазона:
- Устанавливаем курсор в поле «Таблица» в окне построителя формул.

- Возвращаемся к таблице каталога автомобилей.
- Выделяем диапазон с колонками «Модель» и «Цена». У нас получается: А2:Е19
- Теперь выбранную область нужно закрепить. На Windows для этого требуется выбрать значение диапазона в строке ссылок, а затем нажать клавишу F4. На macOS подтверждаем выбранную в строке ссылок область сочетанием клавиш Cmd + T. Это действие необходимо, чтобы функцию можно было протянуть вниз для ее правильного срабатывания во всех строках.
Топ-30 самых востребованных и высокооплачиваемых профессий 2023
Поможет разобраться в актуальной ситуации на рынке труда
Подборка 50+ ресурсов об IT-сфере
Только лучшие телеграм-каналы, каналы Youtube, подкасты, форумы и многое другое для того, чтобы узнавать новое про IT
ТОП 50+ сервисов и приложений от Geekbrains
Безопасные и надежные программы для работы в наши дни
pdf 3,7mb
doc 1,7mb
Уже скачали 19860
Диапазон, который мы установили, появляется в построителе формул и в строке ссылок.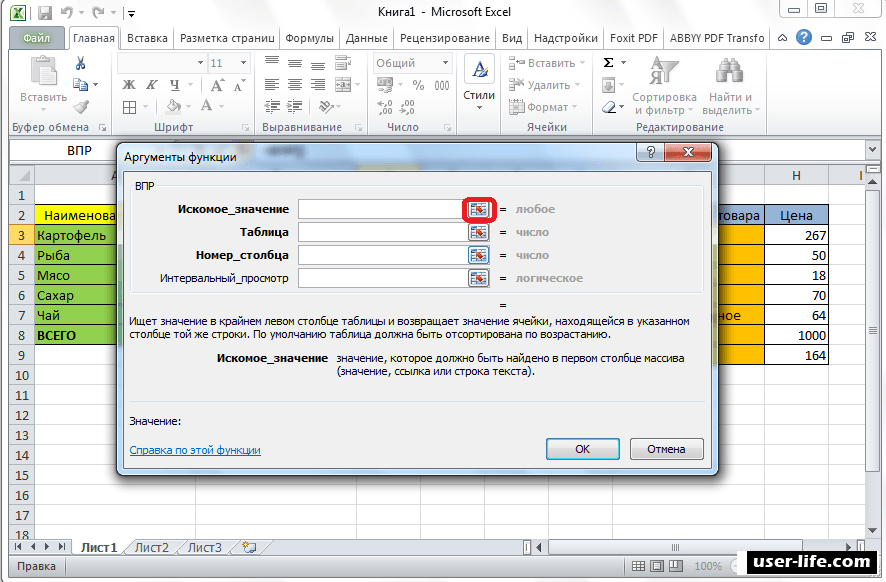 Визуально это выглядит так: fx=ВПР(A2;’каталог авто’!$A$2:$E$19).
Визуально это выглядит так: fx=ВПР(A2;’каталог авто’!$A$2:$E$19).
Номер столбца — это порядковый номер колонки в первой таблице (каталог автомобиль в примере), содержащей значение, которое необходимо перенести во вторую. Счет ведется слева-направо.
Если нумерация колонок не проставлена, необходимо сделать это вручную. У нас столбец «Цена» под номером пять.
Заполнение значений функции
Устанавливаем курсор в поле «Номер столбца» в окне «Построитель формул», вводим нужное значение. Функция ВПР теперь выглядит следующим образом: fx=ВПР(A2;’каталог авто’!$A$2:$E$19;5).
Интервальный просмотр – это параметр настройки работы формулы.
- Если требуется точное совпадение данных, нужно ввести 0.
- Если допускается приближенное значение, ставим 1.
В нашем примере необходим поиск точных значений цены, поэтому выбираем 0.
Значение вводим в поле «Интервальный просмотр» и функция ВПР в Excel приобретает завершенный вид: fx=ВПР(A2;’каталог авто’!$A$2:$E$19;5;0)
Шаг 3.
 Получение результатов
Получение результатов
После всех проделанных действий и установки требуемых аргументов, жмем кнопку «Готово». В ячейке, выделенной нами в первом шаге, появится соответствующее значение – цена модели машины.
Таким образом, мы видим, что функция ВПР в Excel для одной строки сработала. Теперь протягиваем полученное значение вертикально вниз, заставляю формулу работать на оставшихся строчках. С этой целью ранее мы выбрали и закрепили диапазон.
Конечным результатом становится таблица с данными клиентов и информацией о забронированных ими автомобилях. Можно начинать обзвон, не опасаясь путаницы в информации.
Поиск по нескольким критериям
Мы рассмотрели простой ВПР в ExceL, где действовало лишь одно условие. Но может потребоваться сравнение большего количества областей по разным критериям. В таком случае потребуется построение функции ВПР с несколькими условиями.
Давайте попробуем выяснить, например, цену, по которой от ООО «Запад» нам поступил картон. Нужно произвести поиск значений по двум критериям: наименованию материала и поставщику.
Поиск по нескольким критериям
Загвоздка в том, что грузоотправитель доставляет товары разных наименований.
Порядок действий таков:
- В первую очередь нужно добавить в таблицу столбец слева, при этом произведя объединение «Материалов» и «Поставщиков».
- Аналогично совмещаем искомые значения.
- Задаем аргументы для функции ВПР: =ВПР(I6;$A$2:$D$15;4;ЛОЖЬ)
- Нажимаем «Готово». Поиск завершен, цена найдена.
Точный инструмент «Колесо компетенций»
Для детального самоанализа по выбору IT-профессии
Список грубых ошибок в IT, из-за которых сразу увольняют
Об этом мало кто рассказывает, но это должен знать каждый
Мини-тест из 11 вопросов от нашего личного психолога
Вы сразу поймете, что в данный момент тормозит ваш успех
Регистрируйтесь на бесплатный интенсив, чтобы за 3 часа начать разбираться в IT лучше 90% новичков.
Только до 6 марта
Осталось 17 мест
Предположим, что данные по материалам у нас внесены в виде раскрывающегося списка. Тогда настройку функции ВПР в Excel нужно произвести таким образом, чтобы цена отображалась при выборе наименования товара.
Тогда настройку функции ВПР в Excel нужно произвести таким образом, чтобы цена отображалась при выборе наименования товара.
- Создаем раскрывающийся список: устанавливаем курсор в ячейку Е8.
- Переходим во вкладку «Данные» в меню «Проверка данных».
- Тип данных, нужный нам – «Список», для отбора указываем область с названием материалов.
- Подтверждаем свои действия нажатием клавиши «ОК». Раскрывающийся список создан.
Следующий этап – настроить ВПР данных в Excel так, чтобы при выборе конкретного материала переносилась соответствующая ему цена.
Используем «Мастер функций» и устанавливаем аргументы. Искомое значение – ячейка с раскрывающимся списком; таблица – диапазон, включающий в себя «Материалы» и «Цены» (столбец 2). Наша формула должна выглядеть так: =ВПР(E8;A2:B16;2;ЛОЖЬ)
Поиск по нескольким критериям
Подтверждаем настройку нажатием соответствующей клавиши.
Быстрое сравнение двух таблиц с помощью ВПР в Excel
Для обработки информации, содержащейся в объемных таблицах, нет ничего проще и полезней данной функции.
Пример. В связи с изменением прайса, перед нами поставлена задача: произвести сравнение между старыми и новыми ценами.
Для упрощения воспользуемся формулой ВПР в Excel для сравнения:
- Открываем старый прайс и добавляем колонку «Новая цена».
- Встаем на первую ячейку и через «Мастер функций» выбираем ВПР. Задаем параметры и получаем: =ВПР($A$2:$A$15;’новый прайс’!$A$2:$B$15;2;ЛОЖЬ).
- Таким образом мы сделали следующее: указали диапазон наименований А2:А15 в старом прайсе и сравнили его с новым. После чего значения новых цен подставили в ячейку С2 созданного столба прежнего прайса.
С помощью этой функции можно не только проводить сравнительный анализ, но высчитывать разницу в процентах и количестве.
Мы рассказали, как работает функция ВПР в Excel, используя пошаговую инструкцию на конкретном примере. Это полезный инструмент, позволяющий в кратчайшие сроки получить нужный результат. Сначала это может показаться сложным, но уверяем вас: потратив некоторое время на то, чтобы разобраться с формулой, вы сэкономите куда больше.
Рейтинг:
5
( голосов
1 )
Поделиться статьей
как использовать функцию vpr в vs excel
Наверняка многим активным пользователям табличного редактора Excel время от времени приходилось сталкиваться с ситуациями, в которых приходилось подставлять значения из одной таблицы в другую. Только представьте, к вам на склад поступил некий товар. В нашем распоряжении два файла: один с перечнем наименований полученного товара, второй — прайс-лист самого этого товара. Открыв прайс-лист, обнаруживаем, что позиций в нем больше и расположены они не в той последовательности, которая есть в файле со списком наименований. Вряд ли кому-то из нас понравится идея проверять оба файла и переносить цены из одного документа в другой вручную. Конечно, в случае, когда речь идет о 5–10 позициях, механический ввод данных вполне возможен, но что делать, если количество имен превышает 1000? В этом случае Excel и его волшебная функция CDF (или vlookup, если мы говорим об англоязычной версии программы) помогут нам справиться с монотонной работой.
VPR позволяет работать с большими таблицами, перенося данные из одной в другую
Что такое CDF и как им пользоваться?
Итак, в начале нашей работы по преобразованию данных из одной таблицы в другую уместно будет сделать небольшой обзор функции CDF. Как вы, наверное, уже поняли, vlookup позволяет переносить данные из одной таблицы в другую, тем самым автоматически заполняя нужные нам ячейки. Для корректной работы функции CDF обратите внимание на наличие объединенных ячеек в заголовках вашей таблицы. Если они есть, вам нужно будет их сломать.
Предположим, нам необходимо заполнить «Таблицу заказов» данными из «Прайс-листа»
Итак, перед нами стоит задача — перенести цены на существующие товары в таблицу с их наименованиями и посчитать итоговую стоимость каждого продукта. Для этого нам предстоит выполнить следующий алгоритм:
- Сначала приведем таблицу Excel в желаемый вид. Добавьте в подготовленную матрицу данных две колонки с названиями «Цена» и «Стоимость».
 Выберите для ячеек в диапазоне вновь образованных столбцов денежный формат.
Выберите для ячеек в диапазоне вновь образованных столбцов денежный формат. - Теперь активируйте первую ячейку в блоке «Цена» и вызовите «Мастер функций». Это можно сделать, нажав кнопку «fx», расположенную перед строкой формулы, или зажав комбинацию клавиш «Shift+F3». В открывшемся диалоге найдите категорию «Ссылки и массивы». Здесь нас не интересует ничего, кроме функции CDF. Выберите его и нажмите «ОК». Кстати, стоит сказать, что функцию ВПР можно вызвать через вкладку «Формулы», в выпадающем списке которой также находится категория «Связи и массивы».
- После активации CDF вы увидите окно со списком аргументов выбранной вами функции. В поле «Требуемое значение» потребуется ввести диапазон данных, содержащийся в первой колонке таблицы с перечнем полученных товаров и их количеством. То есть нужно сказать Excel, что именно он должен найти во второй таблице и перенести в первую.
- После того, как первый аргумент отмечен, можно перейти ко второму. В нашем случае вторым аргументом является таблица с прайсом.
 Поместите курсор мыши в поле аргумента и перейдите к списку цен. Вручную выделите диапазон с ячейками, расположенными в области столбцов с названиями товарных товаров и их ценой. Укажите Excel, какие значения вы хотите отобразить функциями ВПР.
Поместите курсор мыши в поле аргумента и перейдите к списку цен. Вручную выделите диапазон с ячейками, расположенными в области столбцов с названиями товарных товаров и их ценой. Укажите Excel, какие значения вы хотите отобразить функциями ВПР. - Для того чтобы Excel не путался и ссылался на нужные вам данные, важно исправить указанную на него ссылку. Для этого выделите нужные значения в поле Таблица и нажмите клавишу F4. Если все сделано правильно, на экране должен появиться знак $.
- Теперь переходим в поле аргумента Номер страницы и устанавливаем ему значение «2». Этот блок содержит все данные, которые вы хотите отправить в нашу рабочую таблицу, и поэтому важно присвоить Interval View значение false (установить позицию FALSE). Это нужно для того, чтобы функция VLR работала только с точными значениями, а не округляла их.
Заполните формулу для первого столбца.
Теперь, когда все необходимые действия выполнены, нам остается только подтвердить их нажатием кнопки «ОК». Как только данные в первой ячейке изменятся, нам нужно будет применить функцию CDF ко всему документу Excel. Для этого достаточно распространить ВПР на всю колонку «Цена». Это можно сделать, перетащив правый нижний угол ячейки с измененным значением в самый низ столбца. Если все получилось, и данные изменились так, как нам было нужно, можно переходить к расчету итоговой стоимости нашего товара. Для выполнения этого действия нам нужно найти произведение двух столбцов — «Количества» и «Цены». Так как Excel содержит все математические формулы, расчет может быть предоставлен в «Панель формул» с помощью знакомого значка «fx».
Как только данные в первой ячейке изменятся, нам нужно будет применить функцию CDF ко всему документу Excel. Для этого достаточно распространить ВПР на всю колонку «Цена». Это можно сделать, перетащив правый нижний угол ячейки с измененным значением в самый низ столбца. Если все получилось, и данные изменились так, как нам было нужно, можно переходить к расчету итоговой стоимости нашего товара. Для выполнения этого действия нам нужно найти произведение двух столбцов — «Количества» и «Цены». Так как Excel содержит все математические формулы, расчет может быть предоставлен в «Панель формул» с помощью знакомого значка «fx».
Важный момент
Казалось бы все готово и ВПР справился с нашей задачей, но не тут то было. Дело в том, что в столбце «Цена» функция CDF еще активна, свидетельством этого факта является отображение последней в строке формул. То есть обе наши таблицы остаются связанными друг с другом. Такой тандем может привести к тому, что при изменении данных в таблице с ценой меняется и информация, содержащаяся в нашем рабочем файле со списком товаров.
Лучше всего избежать этой ситуации, разделив две таблицы. Для этого нам нужно выделить ячейки, которые находятся в диапазоне столбца Цена, и щелкнуть по нему правой кнопкой мыши. В открывшемся окне выберите и активируйте опцию «Копировать». После этого, не снимая выделение с выделенной области ячейки, снова нажмите правую кнопку мыши и выберите опцию «Специальная вставка».
При включении этой опции на вашем экране откроется диалоговое окно, в котором вам нужно будет установить флажок рядом с категорией «Значение». Подтвердите свои действия, нажав на кнопку «ОК».
Возвращаемся к нашей строке формул и проверяем наличие активной функции ВПР в столбце Цена. Если на месте формулы вы видите только числовые значения, то все получилось, а функция CDF отключена. То есть связь между двумя файлами Excel разрывается, и нет угрозы незапланированного изменения или удаления данных, прикрепленных к таблице с прайс-листом. Теперь вы можете спокойно пользоваться табличным документом и не беспокоиться о том, что будет, если Прайс-лист закроют или перенесут в другое место.
Перетащите маркер в правом нижнем углу ячейки, чтобы применить формулу ко всей таблице.
Как сравнить две таблицы в Excel?
С помощью функции CDF можно за считанные секунды сравнить несколько разных значений, чтобы, например, сравнить, как изменились цены на уже существующий товар. Для этого нужно прописать ВПР в пустой столбец и связать функцию с измененными значениями, которые находятся в другой таблице. Лучше всего, если столбец «Новая цена» будет располагаться сразу за столбцом «Цена». Такое решение позволит вам сделать изменение цены более заметным для сравнения.
Возможность работы с несколькими условиями
Еще одним несомненным преимуществом функции ВПР является возможность работы с несколькими параметрами, присущими вашему продукту. Для поиска товара по двум и более характеристикам необходимо:
- Создать два (или, при необходимости, больше) условия поиска.
- Добавить новую колонку, к которой в процессе работы функции будут добавляться все остальные колонки, по которым осуществляется поиск товара.

- В полученный столбец по описанному выше алгоритму вводим уже знакомую нам формулу функции ВПР.
В заключение следует сказать, что поддержание в Excel такой функции, как CDF, значительно упрощает работу с табличной информацией. Не бойтесь использовать ВПР в работе с огромным объемом данных, ведь как бы они ни выполнялись, принцип работы функции всегда один и тот же. Все, что вам нужно сделать, это правильно определить его аргументы.
Функция ВПР. Использование функции ВПР. Excel
Приложение Excel популярно благодаря своей доступности и простоте, так как не требует специальных знаний и навыков. Табличный вид предоставления информации понятен любому пользователю, а широкий набор инструментов, включая «Мастер функций», позволяет производить любые манипуляции и расчеты с предоставленными данными.
Одной из известных формул Excel является вертикальный просмотр. Использование функции VLOOK на первый взгляд кажется довольно сложным, но это только на первый взгляд.
Как работает Excel
При работе с формулой VLR следует учитывать, что она ищет искомое значение исключительно по столбцам, а не по строкам. Для использования функции необходимо минимальное количество столбцов — два, максимальное отсутствует.
Функция VLOOK ищет в таблице заданный критерий, который может иметь любой формат (текстовый, числовой, денежный, дата и время и т.д.). В случае нахождения записи выводит (подставляет) значение, введенное в той же строке, но из нужного столбца таблицы, то есть соответствующее заданному критерию. Если искомое значение не найдено, то выводится ошибка #N/A (в английской версии #N/A).
Необходимо использовать
Функция ВПР приходит на помощь оператору, когда требуется быстро найти и применить определенное значение из таблицы большего размера в дальнейших расчетах, анализе или прогнозировании. Главное при использовании этой формулы – убедиться, что указанная область поиска выбрана правильно. В него должны быть включены все записи, то есть от первой до последней.
Самый распространенный случай использования VLOOK (функция Excel) — сравнение или сложение данных в двух таблицах по определенному критерию. Причем диапазоны поиска могут быть большими и вмещать тысячи полей, размещенных на разных листах или книгах.
Показана функция VLF, как ею пользоваться, как выполнять расчеты, в качестве примера на рисунке выше. Вот таблица размеров розничных продаж в зависимости от региона и менеджера. Критерий поиска — конкретный менеджер (его имя и фамилия), а искомое значение — сумма его продаж.
В результате функции ВПР создается новая таблица, в которой конкретный рассматриваемый менеджер быстро сравнивает свои суммы продаж.
Алгоритм заполнения формулы
Формула VLOOK находится на вкладке «Мастер функций» и в разделе «Ссылки и массивы». Диалог функции имеет следующий вид:
Аргументы в формулу вводятся в порядке очереди:
- Значение поиска — это то, что должна найти функция, а варианты — значения ячейки, ее адрес, имя дается ему оператором.
 В нашем случае это фамилия и имя менеджера.
В нашем случае это фамилия и имя менеджера. - Таблица — диапазон строк и столбцов, в которых ищется критерий.
- Номер столбца – это его порядковый номер, в котором находится сумма продаж, то есть результат работы формулы.
- Интервальный вид. Он содержит значение FALSE или TRUE. Причем FALSE возвращает только точное совпадение, TRUE — позволяет искать приблизительное значение.
Пример использования функции
Функция ВПР может иметь следующий пример: при работе с бизнесом в таблице Excel в столбце А указано название продукта, а в столбце В — соответствующая цена. Чтобы написать предложение в колонке C, вам нужно найти стоимость определенного товара, который вы хотите вывести в колонке D.
| A | AT | FROM | D |
| Product 1 | 90 | Product 3 | 60 |
| Product 2 | 120 | Продукт 1 | 90 |
| Продукт 3 | 60 | Продукт 4 | 100 |
| 0129 | Товар 2 | 120 |
Формула, записанная на D, будет выглядеть так: =ВПР(С1,А1:В5;2;0), то есть ВПР(поисковое значение, диапазон данных таблицы, порядковый номер столбца, 0). В качестве четвертого аргумента вместо 0 можно использовать ЛОЖЬ.
В качестве четвертого аргумента вместо 0 можно использовать ЛОЖЬ.
Для заполнения таблицы предложения полученную формулу необходимо скопировать на весь столбец D.
Для фиксации области рабочего диапазона данных можно использовать абсолютные ссылки. Для этого знаки $ ставятся вручную перед буквенными и числовыми значениями адресов крайних левой и правой ячеек таблицы. В нашем случае формула принимает вид: =ВПР(С1;$А$1:$В$5;2;0).
Ошибки при использовании
Функция ВПР не работает, после чего в столбце вывода результата ошибки появляется сообщение (# Н/Д или # Н/Д). Это бывает в таких случаях:
- Формула введена, а столбец требуемых критериев не заполнен (в данном случае столбец С).
- Столбец C содержит значение, отсутствующее в столбце A (в диапазоне поиска данных). Чтобы проверить наличие нужного значения, выберите столбец критериев и на вкладке «Правка» — «Найти» вставьте эту запись, запустите поиск. Если программа его не находит, значит он отсутствует.

- Форматы ячеек столбцов А и С (обязательные критерии) разные, например, у одного текстовый, а у другого числовой. Вы можете изменить формат ячейки, если перейдете к редактированию ячейки (F2). Такие проблемы обычно возникают при импорте данных из других приложений. Во избежание таких ошибок в формулу VLOOK можно встроить следующие функции: KEY или TEXT. Выполнение этих алгоритмов автоматически преобразует формат ячеек.
- В коде функции есть непечатаемые символы или пробелы. Затем следует внимательно проверить формулу на наличие ошибок ввода.
- Задан приблизительный поиск, то есть четвертый аргумент функции ВПР имеет значение 1 или ИСТИНА, а таблица не отсортирована по возрастанию. В этом случае столбец искомых критериев должен быть отсортирован по возрастанию.
Кроме того, при организации новой сводной таблицы заданные обязательные критерии могут быть в любом порядке и последовательности и не обязательно должны содержаться в полном списке (частичный выбор).
Особенности использования в качестве интервального просмотра 1 или TRUE
Ошибка под номером 5 довольно распространена и наглядно показана на рисунке ниже.
В данном примере список имен по нумерации отсортирован не по возрастанию, а по убыванию. А в качестве интервального просмотра использовался критерий ИСТИНА (1), который сразу прерывает поиск при нахождении значения большего, чем искомое, поэтому выдается ошибка.
При применении 1 или TRUE в четвертом аргументе необходимо убедиться, что столбец с искомыми критериями отсортирован по возрастанию. При использовании 0 или FAL эта необходимость отпадает, но и возможности интервального сканирования тоже нет.
Только имейте в виду, что особенно важно сортировать таблицы интервалов. В противном случае функция ВПР будет выводить в ячейки некорректные данные.
Другие нюансы при работе с функцией ВПР
Для удобства работы с такой формулой можно озаглавить диапазон таблицы, в которой производится поиск (второй аргумент), как показано на рисунке.
В этом случае область стола продаж имеет право. Для этого выбирается таблица, за исключением заголовков столбцов, и указывается имя в поле имени (слева под панелью вкладок).
Еще один вариант — заголовок — подразумевает выделение диапазона данных, затем переход в меню «Вставка» — «Имя» — «Назначить».
Для того чтобы использовать данные, размещенные на другом листе рабочей книги, с помощью функции ВПР необходимо во втором аргументе формулы указать расположение диапазона данных. Например, =ВПР(А1;Список2!$А$1:$В$5;2;0), где Лист2! — это ссылка на нужный лист книги, а $A$1:$B$5 — адрес диапазона извлечения данных.
Пример организации учебного процесса с ВЛЧ
В Excel достаточно удобно использовать функцию ВПР не только для фирм, занимающихся торговлей, но и для образовательных учреждений для оптимизации процесса сравнения учащихся (студентов) с их оценки. Примеры таких задач показаны на рисунках ниже.
Есть две таблицы со списками учеников. Один со своими оценками, второй указывает на возраст. Необходимо сопоставить обе таблицы, чтобы наряду с возрастом учащихся были выведены их оценки, то есть ввести дополнительный столбец во второй список.
Один со своими оценками, второй указывает на возраст. Необходимо сопоставить обе таблицы, чтобы наряду с возрастом учащихся были выведены их оценки, то есть ввести дополнительный столбец во второй список.
Функция VLOOK отлично справляется с решением этой задачи. В столбце Г под заголовком «Оценки» записывается соответствующая формула: = ВПР(Э4, В3: С13, 2, 0). Его необходимо скопировать на весь столбец таблицы.
В результате функция VLR выдаст оценки, полученные некоторыми учащимися.
Пример организации поисковой системы с ВПР
Еще одним примером использования функции ВПР является организация поисковой системы, когда в базе данных по заданному критерию необходимо найти соответствующее ему значение . Таким образом, на рисунке показан список с кличками животных и их принадлежностью к тому или иному виду.
С помощью ВЛР создается новая таблица, в которой легко найти кличку по кличке животного. Эти поисковики актуальны при работе с большими списками. Чтобы не пересматривать вручную все записи, можно быстро воспользоваться поиском и получить нужный результат.
Чтобы не пересматривать вручную все записи, можно быстро воспользоваться поиском и получить нужный результат.
ZBTB2 подавляет транскрипцию ВИЧ-1 и регулируется Vpr ВИЧ-1 и реакцией на повреждение клеточной ДНК . Дж. Лейкок Биол
2003;74(5):736–49.. 10.1189/jlb.0403180 . [PubMed] [CrossRef] [Google Scholar]
2. Перейра Л.А., Бентли К., Питерс А., Черчилль М.Дж., Дикон Н.Дж. Подборка взаимодействий клеточных факторов транскрипции с промотором LTR ВИЧ-1. Нуклеиновые Кислоты Res
2000;28(3):663–8. 10.1093/нар/28.3.663 . [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
3. Kao SY, Calman AF, Luciw PA, Peterlin BM. Антитерминация транскрипции в длинном концевом повторе ВИЧ-1 с помощью продукта гена tat. Природа
1987;330(6147):489–93. 10.1038/330489а0. [PubMed] [CrossRef] [Google Scholar]
4. Zhu Y, Pe’ery T, Peng J, Ramanathan Y, Marshall N, Marshall T, et al. Фактор элонгации транскрипции P-TEFb необходим для трансактивации tat ВИЧ-1 in vitro. Гены Дев
1997;11(20):2622–32. 10.1101/гад.11.20.2622. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
10.1101/гад.11.20.2622. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
5. He N, Zhou Q. Новое понимание контроля транскрипции ВИЧ-1: когда Tat встречается с 7SK snRNP и комплексом суперэлонгации (SEC).
J Нейроиммун Фармакол
2011;6(2):260–8. Эпублик 2011/03/02. 10.1007/с11481-011-9267-6
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
6. Goh WC, Rogel ME, Kinsey CM, Michael SF, Fultz PN, Nowak MA, et al. Vpr ВИЧ-1 увеличивает экспрессию вируса, манипулируя клеточным циклом: механизм селекции Vpr in vivo. Нат Мед
1998;4(1):65–71. 10.1038/nm0198-065. [PubMed] [CrossRef] [Google Scholar]
7. Савайя Б.Е., Халили К., Гордон Дж., Таубе Р., Амини С. Совместное взаимодействие между регуляторными белками ВИЧ-1 Tat и Vpr модулирует транскрипцию вирусного генома. J Биол Хим
2000;275(45):35209–14. 10.1074/jbc.M005197200 . [PubMed] [CrossRef] [Google Scholar]
8. Kashanchi F, Agbottah ET, Pise-Masison CA, Mahieux R, Duvall J, Kumar A, et al. Регулируемая клеточным циклом транскрипция трансактиватором Tat вируса иммунодефицита человека 1 типа. Дж Вирол. 2000;74(2):652–60. 10.1128/jvi.74.2.652-660.2000
Регулируемая клеточным циклом транскрипция трансактиватором Tat вируса иммунодефицита человека 1 типа. Дж Вирол. 2000;74(2):652–60. 10.1128/jvi.74.2.652-660.2000
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
9. Guenzel CA, Herate C, Benichou S. ВИЧ-1 Vpr-все еще «загадочный многозадачный».
Фронт микробиол
2014;5:127. 10.3389/fmicb.2014.00127
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
10. Gonzalez ME. Белок Vpr ВИЧ-1: многогранная мишень для терапевтического вмешательства.
Int J Mol Sci.
2017;18(1). 10.3390/ijms18010126
[Статья бесплатно PMC] [PubMed] [CrossRef] [Google Scholar]
11. Dehart JL, Planelles V. Вирус иммунодефицита человека типа 1 Vpr связывает деградацию протеасом и активацию контрольных точек. Джей Вирол
2008;82(3):1066–72. 10.1128/ОВИ.01628-07
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
12. DeHart JL, Zimmerman ES, Ardon O, Monteiro-Filho CM, Arganaraz ER, Planelles V. Vpr ВИЧ-1 активирует контрольную точку G2 путем манипулирования протеасомной системой убиквитина.
Вирол Дж.
2007; 4:57. 10.1186/1743-422С-4-57
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
13. Hrecka K, Gierszewska M, Srivastava S, Kozaczkiewicz L, Swanson SK, Florens L, et al. Лентивирусный Vpr узурпирует убиквитинлигазу Cul4-DDB1 [VprBP] E3 для модуляции клеточного цикла. Proc Natl Acad Sci U S A. 2007;104(28):11778–83. 10.1073/пнас.0702102104
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
14. Le Rouzic E, Belaidouni N, Estrabaud E, Morel M, Rain JC, Transy C, et al. Vpr ВИЧ1 останавливает клеточный цикл, рекрутируя DCAF1/VprBP, рецептор убиквитинлигазы Cul4-DDB1. Клеточный цикл. 2007;6(2):182–8. 10.4161/cc.6.2.3732. [PubMed] [CrossRef] [Google Scholar]
15. Романи Б., Байглу Н.С., Хамиди-Фард М., Агасадеги М.Р., Аллахбахши Э. Белок Vpr ВИЧ-1 индуцирует протеасомную деградацию связанных с хроматином хроматин-ассоциированных HDAC класса I для преодоления латентной инфекции макрофагов. J Биол Хим
2016;291(6):2696–711. 10.1074/jbc. M115.689018
M115.689018
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
16. Романи Б., Камали Джамиль Р., Хамиди-Фард М., Рахими П., Момен С.Б., Агасадеги М.Р. и др. Vpr ВИЧ-1 реактивирует латентный провирус ВИЧ-1, вызывая истощение HDAC класса I на хроматине.
Научный представитель
2016;6:31924. 10.1038/srep31924
[PMC free article] [PubMed] [CrossRef] [Google Scholar]
17. Романи Б., Шейх Байглу Н., Агасадеги М.Р., Аллахбахши Э. Белок Vpr ВИЧ-1 усиливает протеасомную деградацию фактора репликации ДНК MCM10 через Cul4-DDB1 [VprBP] Убиквитинлигаза E3 вызывает остановку клеточного цикла G2/M. J Биол Хим
2015;290 (28): 17380–9. 10.1074/jbc.M115.641522
[PMC free article] [PubMed] [CrossRef] [Google Scholar]
18. Fregoso OI, Emerman M. Активация реакции на повреждение ДНК является консервативной функцией ВИЧ-1 и ВИЧ-2 Vpr, которая не зависит от набора SLX4 .
Мбио. 2016;7(5). АРТН e01433-16 WOS:0003
8. 10.1128/мБио.01433-16
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
19. Рошал М., Ким Б., Чжу Ю., Нгием П., Планеллес В. Активация ATR-опосредованного ответа на повреждение ДНК вирусным белком ВИЧ-1 Р. Дж. Биол Хим
Рошал М., Ким Б., Чжу Ю., Нгием П., Планеллес В. Активация ATR-опосредованного ответа на повреждение ДНК вирусным белком ВИЧ-1 Р. Дж. Биол Хим
2003;278(28):25879–86. 10.1074/jbc.M303948200 . [PubMed] [CrossRef] [Google Scholar]
20. Zhu Y, Gelbard HA, Roshal M, Pursell S, Jamieson BD, Planelles V. Сравнение остановки клеточного цикла, трансактивации и апоптоза, вызванных вирусом иммунодефицита обезьян SIVagm и гены vpr вируса иммунодефицита человека 1 типа. Джей Вирол
2001;75(8):3791–801. 10.1128/ОВИ.75.8.3791-3801.2001
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
21. Valerie K, Delers A, Bruck C, Thiriart C, Rosenberg H, Debouck C, et al. Активация вируса иммунодефицита человека типа 1 путем повреждения ДНК в клетках человека. Природа. 1988;333(6168):78–81. 10.1038/333078а0. [PubMed] [CrossRef] [Google Scholar]
22. Faure E, Cavard C, Zider A, Guillet JP, Resbeut M, Champion S. Индуцированная облучением X транскрипция длинного терминального повтора ВИЧ 1 типа. СПИД Рес Хум Ретровир
СПИД Рес Хум Ретровир
1995;11(1):41–3. 10.1089/помощь.1995.11.41. [PubMed] [CrossRef] [Google Scholar]
23. Smith RA, Ingels J, Lochemes JJ, Dutkowsky JP, Pifer LL. Гамма-облучение ВИЧ-1. J Ортоп Рес
2001;19(5):815–9. 10.1016/S0736-0266(01)00018-3. [PubMed] [CrossRef] [Академия Google]
24. Sadaie MR, Tschachler E, Valerie K, Rosenberg M, Felber BK, Pavlakis GN, et al. Активация tat-дефектного вируса иммунодефицита человека ультрафиолетовым светом. Нью Биол
1990;2(5):479–86. . [PubMed] [Google Scholar]
25. Laguette N, Bregnard C, Hue P, Basbous J, Yatim A, Larroque M, et al. Преждевременная активация комплекса SLX4 с помощью Vpr способствует аресту G2/M и ускользанию от врожденного иммунного восприятия. Клетка. 2014;156(1–2):134–45. 10.1016/j.cell.2013.12.011. [PubMed] [CrossRef] [Академия Google]
26. Bregnard C, Benkirane M, Laguette N. Механизм восстановления повреждений ДНК и ускользание ВИЧ от врожденного иммунного восприятия. Фронт микробиол
2014;5:176. 10.3389/fmicb.2014.00176
10.3389/fmicb.2014.00176
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
27. Sadowski I, Lourenco P, Malcolm T. Факторы, контролирующие организацию хроматина и расположение нуклеосом для установления и поддержания латентности ВИЧ.
Текущая резистентность к ВИЧ
2008;6(4):286–95. 10.2174/157016208785132563 . [PubMed] [CrossRef] [Академия Google]
28. Уильямс С.А., Грин В.К. Регуляция латентности ВИЧ-1 путем активации Т-клеток. Цитокин
2007;39(1):63–74. 10.1016/j.cyto.2007.05.017. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
29. Richman DD, Margolis DM, Delaney M, Greene WC, Hazuda D, Pomerantz RJ. Проблема поиска лекарства от ВИЧ-инфекции. Наука
2009;323(5919):1304–7. 10.1126/наука.1165706. [PubMed] [CrossRef] [Google Scholar]
30. Razooky BS, Pai A, Aull K, Rouzine IM, Weinberger LS. Запрограммированная программа латентности ВИЧ. Клетка
2015;160(5):990–1001. 10.1016/j.cell.2015.02.009
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
31. Вайнбергер Л.С., Шенк Т. Резистор обратной связи ВИЧ: деактиватор схемы саморегуляции и шумовой буфер. ПЛОС Биол
Вайнбергер Л.С., Шенк Т. Резистор обратной связи ВИЧ: деактиватор схемы саморегуляции и шумовой буфер. ПЛОС Биол
2007;5(1):e9. 10.1371/journal.pbio.0050009
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
32. Manome Y, Yao XJ, Kufe DW, Cohen EA, Fine HA. Избирательное воздействие агентов, повреждающих ДНК, на активацию длинных терминальных повторов ВИЧ и репликацию вируса in vitro. J Acquir Immune Defic Syndr Hum Retrovirol
1996;11(2):109–16. 10.1097/00042560-199602010-00001. [PubMed] [CrossRef] [Google Scholar]
33. Stanley SK, Folks TM, Fauci AS. Индукция экспрессии вируса иммунодефицита человека в хронически инфицированной промоноцитарной клеточной линии ультрафиолетовым облучением. СПИД Рес Хум Ретровир
1989;5(4):375–84. 10.1089/помощь.1989.5.375. [PubMed] [CrossRef] [Google Scholar]
34. Vicenzi E, Poli G. Ультрафиолетовое облучение и цитокины как регуляторы латентности и экспрессии ВИЧ. Химия Биол Взаимодействие
1994;91(2–3):101–9. 10.1016/0009-2797(94)
-2 . [PubMed] [CrossRef] [Google Scholar]
[PubMed] [CrossRef] [Google Scholar]
35. Леви Д.Н., Рафаэли И., МакГрегор Р.Р., Вайнер Д.Б. Сывороточный Vpr регулирует продуктивную инфекцию и латентность вируса иммунодефицита человека типа 1. Proc Natl Acad Sci U S A
1994; 91 (23): 10873–7. 10.1073/пнас.91.23.10873
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
36. Леви Д.Н., Рафаэли Ю., Вайнер Д.Б. Внеклеточный белок Vpr повышает восприимчивость клеток к репликации вируса иммунодефицита человека и реактивирует вирус из латентного состояния. Джей Вирол
1995;69(2):1243–52. 10.1128/ОВИ.69.2.1243-1252.1995
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
37. Schwartz C, Bouchat S, Marban C, Gautier V, Van Lint C, Rohr O, et al. На пути к излечению: очистка латентных резервуаров ВИЧ-1. Биохим Фармакол. 2017. 10.1016/j.bcp.2017.07.001. [PubMed] [CrossRef] [Google Scholar]
38. Bruce JW, Reddington R, Mathieu E, Bracken M, Young JA, Ahlquist P. ZASC1 стимулирует удлинение транскрипции ВИЧ-1 путем привлечения P-TEFb и TAT к промотору LTR. .
.
PLoS Патог
2013;9(10):e1003712. Эпублик 2013/11/10. 10.1371/журнал.ppat.1003712
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
39. Chiang WF, Hung PS, Liu SY, Yuan TC, Chang KW, Chen YP, et al. Увеличение числа копий гена ZASC1 при рецидивирующей карциноме полости рта. Оральный Дис. 2011;17(1):53–9. Эпублик 22.07.2010. 10.1111/j.1601-0825.2010.01702.x . [PubMed] [CrossRef] [Google Scholar]
40. Imoto I, Yuki Y, Sonoda I, Ito T, Shimada Y, Imamura M, et al. Идентификация ZASC1, кодирующего белок цинкового пальца Круппеля, в качестве новой мишени для амплификации 3q26 при плоскоклеточном раке пищевода. Рак Рез
2003;63(18):5691–6. . [PubMed] [Google Scholar]
41. Lin SC, Liu CJ, Ko SY, Chang HC, Liu TY, Chang KW. Амплификация числа копий онкогенов 3q26-27 в микрорассеченной плоскоклеточной карциноме полости рта и в образцах, обработанных щеткой полости рта от жевательных ареков. Дж. Патол
2005;206(4):417–22. 10.1002/путь.1790 . [PubMed] [CrossRef] [Google Scholar]
42. Чириелло Г., Миллер М.Л., Аксой Б.А., Сенбабаоглу Ю., Шульц Н., Сандер С. Возникающий ландшафт онкогенных сигнатур рака человека. Нат Жене
Чириелло Г., Миллер М.Л., Аксой Б.А., Сенбабаоглу Ю., Шульц Н., Сандер С. Возникающий ландшафт онкогенных сигнатур рака человека. Нат Жене
2013;45(10):1127–33. 10.1038/нг.2762
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
43. Lim J, Hao T, Shaw C, Patel AJ, Szabo G, Rual JF, et al. Сеть белок-белковых взаимодействий для наследственных атаксий человека и нарушений дегенерации клеток Пуркинье. Клетка
2006;125(4):801–14. 10.1016/j.cell.2006.03.032. [PubMed] [CrossRef] [Google Scholar]
44. Bogaerts S, Vanlandschoot A, van Hengel J, van Roy F. Ядерная транслокация альфа-N-катенина новым репрессором транскрипции цинковых пальцев ZASC1. Разрешение ячейки опыта
2005;311(1):1–13. 10.1016/j.yexcr.2005.06.018. [PubMed] [CrossRef] [Академия Google]
45. Bruce JW, Hierl M, Young JA, Ahlquist P. Фактор клеточной транскрипции ZASC1 регулирует транскрипцию вируса мышиного лейкоза. Джей Вирол
2010;84(15):7473–83. Эпб 2010/05/21. 10.1128/ОВИ.00299-10
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
46. Юнг С.Ю., Малованная А., Вей Дж., О’Мэлли Б.В., Цинь Дж. Протеомный анализ стационарных комплексов коактиватора ядерного гормонального рецептора. Мол Эндокринол
Юнг С.Ю., Малованная А., Вей Дж., О’Мэлли Б.В., Цинь Дж. Протеомный анализ стационарных комплексов коактиватора ядерного гормонального рецептора. Мол Эндокринол
2005;19(10):2451–65. 10.1210/me.2004-0476. [PubMed] [CrossRef] [Академия Google]
47. Ван Нуланд Р., Смитс А.Х., Паллаки П., Янсен П.В., Вермеулен М., Тиммерс Х.Т. Количественное рассечение и определение стехиометрии комплексов гистон-метилтрансферазы SET1/MLL человека. Мол Селл Биол. 2013;33(10):2067–77. 10.1128/МКБ.01742-12
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
48. Joshi P, Greco TM, Guise AJ, Luo Y, Yu F, Nesvizhskiy AI, et al. Функциональный ландшафт интерактома семейства гистоновых деацетилаз человека. Мол Сист Биол. 2013;9:672. 10.1038/msb.2013.26
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
49. Siggs OM, Beutler B. Факторы транскрипции BTB-ZF. Клеточный цикл
2012;11(18):3358–69. 10.4161/cc.21277
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
50. Lee SU, Maeda TPOK. Белки ZBTB: новое семейство белков, которые регулируют развитие и функцию лимфоидной ткани. Immunol Rev. 2012; 247:107–19. 10.1111/j.1600-065X.2012.01116.x WOS:000302796600009. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Lee SU, Maeda TPOK. Белки ZBTB: новое семейство белков, которые регулируют развитие и функцию лимфоидной ткани. Immunol Rev. 2012; 247:107–19. 10.1111/j.1600-065X.2012.01116.x WOS:000302796600009. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
51. Jeon BN, Choi WI, Yu MY, Yoon AR, Kim MH, Yun CO, et al. ZBTB2, новый мастер-регулятор пути p53. Дж. Биол. Хим. 2009 г.;284(27):17935–46. 10.1074/jbc.M809559200
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
52. Kim MY, Koh DI, Choi WI, Jeon BN, Jeong DY, Kim KS, et al. ZBTB2 увеличивает экспрессию PDK4 за счет репрессии транскрипции RelA/p65. Нуклеиновые Кислоты Res. 2015;43(3):1609–25. 10.1093/нар/гкв026
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
53. Gylfe AE, Kondelin J, Turunen M, Ristolainen H, Katainen R, Pitkanen E, et al. Идентификация онкогенов-кандидатов при колоректальном раке человека с микросателлитной нестабильностью. Гастроэнтерология. 2013;145(3):540–3 e22. 10.1053/j.gastro.2013.05.015. [PubMed] [CrossRef] [Академия Google]
10.1053/j.gastro.2013.05.015. [PubMed] [CrossRef] [Академия Google]
54. Wang Y, Zheng X, Zhang Z, Zhou J, Zhao G, Yang J, et al. МикроРНК-149 ингибирует пролиферацию и развитие клеточного цикла путем нацеливания на ZBTB2 при раке желудка человека.
ПЛОС Один.
2012;7(10):e41693. 10.1371/journal.pone.0041693
[Статья PMC бесплатно] [PubMed] [CrossRef] [Google Scholar]
55. Zheng W, Long J, Gao YT, Li C, Zheng Y, Xiang YB, et al. Полногеномное ассоциативное исследование идентифицирует новый локус предрасположенности к раку молочной железы в 6q25.1. Нат Жене. 2009;41(3):324–8. 10.1038/нг.318
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
56. Boireau S, Maiuri P, Basyuk E, de la Mata M, Knezevich A, Pradet-Balade B, et al. Цикл транскрипции ВИЧ-1 в реальном времени и в живых клетках. Джей Селл Биол. 2007;179(2):291–304. Эпублик 24.10.2007. 10.1083/jcb.200706018
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
57. Molle D, Maiuri P, Boireau S, Bertrand E, Knezevich A, Marcello A, et al. Просмотр в реальном времени комплекса TAR:Tat:P-TEFb в сайтах транскрипции ВИЧ-1.
Просмотр в реальном времени комплекса TAR:Tat:P-TEFb в сайтах транскрипции ВИЧ-1.
Ретровирусология. 2007; 4:36. Эпублик 2007/06/01. 10.1186/1742-4690-4-36
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
58. Батлер С.Л., Хансен М.С., Бушман Ф.Д. Количественный анализ интеграции ДНК ВИЧ in vivo. Нат Мед
2001;7(5):631–634. Эпублик 01.05.2001. 10.1038/87979. [PubMed] [CrossRef] [Google Scholar]
59. Jones KA, Kadonaga JT, Luciw PA, Tjian R. Активация промотора ретровируса СПИДа клеточным фактором транскрипции Sp1
Наука
1986; 232 (4751): 755–9. 10.1126/науки.3008338. [PubMed] [CrossRef] [Академия Google]
60. Murry JP, Godoy J, Mukim A, Swann J, Bruce JW, Ahlquist P, et al. Ингибиторы пути сульфирования блокируют реактивацию латентного ВИЧ-1. Вирусология. 2014; 471–473:1–12. 10.1016/ж.вирол.2014.08.016
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
61. Эль Харруби А., Пирас Г., Зенсен Р., Мартин М.А. Транскрипционная активация встроенного промотора вируса иммунодефицита человека типа 1, ассоциированного с хроматином. Мол Селл Биол. 1998;18(5):2535–44. Эпб 1998/05/05. 10.1128/мкб.18.5.2535
Мол Селл Биол. 1998;18(5):2535–44. Эпб 1998/05/05. 10.1128/мкб.18.5.2535
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
62. Van Lint C, Emiliani S, Verdin E. Экспрессия небольшой части клеточных генов изменяется в ответ на гиперацетилирование гистонов. Джин Экспр. 1996;5(4–5):245–53. Эпб 1996/01/01. [Статья бесплатно PMC] [PubMed] [Google Scholar]
63. Verdin E, Paras P Jr., Van Lint C. Нарушение хроматина в промоторе вируса иммунодефицита человека типа 1 во время активации транскрипции. ЭМБО J
1993;12(8):3249–59. Эпб 1993/08/01. [Бесплатная статья PMC] [PubMed] [Google Scholar]
64. Pietrzak M, Halicka HD, Wieczorek Z, Wieczorek J, Darzynkiewicz Z. Ослабление взаимодействия акридинового мутагена ICR-191 с ДНК и повреждение ДНК перехватчиком мутагена хлорофиллином. Биофиз Хим
2008;135(1–3):69–75. Эпб 2008/04/22. 10.1016/j.bpc.2008.03.004
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
65. Kawasumi M, Bradner JE, Tolliday N, Thibodeau R, Sloan H, Brummond KM, et al. Идентификация ингибиторов пути ATR-Chk1, которые избирательно нацелены на клетки с дефицитом p53, не подавляя непосредственно каталитическую активность ATR. Рак рез. 2014;74(24):7534–45. Эпублик 23.10.2014. 10.1158/0008-5472.CAN-14-2650
Идентификация ингибиторов пути ATR-Chk1, которые избирательно нацелены на клетки с дефицитом p53, не подавляя непосредственно каталитическую активность ATR. Рак рез. 2014;74(24):7534–45. Эпублик 23.10.2014. 10.1158/0008-5472.CAN-14-2650
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
66. Трикетт А., Кван Ю.Л. Стимуляция и размножение Т-клеток с использованием гранул анти-CD3/CD28. J Иммунол Методы
2003;275(1–2):251–5. Эпб 2003/04/02. 10.1016/s0022-1759(03)00010-3 . [PubMed] [CrossRef] [Google Scholar]
67. Martin M, Kettmann R, Dequiedt F. Деацетилазы гистонов класса IIa: регулирование регуляторов. Онкоген
2007;26(37):5450–67. 10.1038/sj.onc.1210613 . [PubMed] [CrossRef] [Google Scholar]
68. Wright LH, Menick DR. Собственный класс: изучение недеацетилазной роли HDAC класса IIa в сердечно-сосудистых заболеваниях. Am J Physiol Heart Circ Physiol
2016;311(1):h299–206. 10.1152/ajpheart.00271.2016
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
69. Парра М.
Парра М.
HDAC класса IIa — новый взгляд на их функции в физиологии и патологии. ФЕБС Дж
2015; 282(9):1736–44. 10.1111/февраль 13061 . [PubMed] [CrossRef] [Google Scholar]
70. Li J, Chen J, Ricupero CL, Hart RP, Schwartz MS, Kusnecov A, et al. Накопление в ядре HDAC4 при дефиците АТМ способствует нейродегенерации при атаксии-телеангиэктазии. Нат Мед. 2012;18(5):783–90. 10.1038/нм.2709[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
71. Kulkarni A, Wilson DM, 3rd. Участие повреждений ДНК и дефектов репарации в неврологической дисфункции. Am J Hum Genet
2008;82(3):539–66. 10.1016/j.ajhg.2008.01.009
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
72. Paulson HL, Miller VM. Нарушения координации: восстановление ДНК при наследственной атаксии. Нейрон
2005;46(6):845–8. 10.1016/j.neuron.2005.05.025. [PubMed] [CrossRef] [Google Scholar]
73. Poon B, Grovit-Ferbas K, Stewart SA, Chen IS. Остановка клеточного цикла с помощью Vpr в вирионах ВИЧ-1 и нечувствительность к антиретровирусным препаратам. Наука
Наука
1998;281(5374):266–9. 10.1126/наука.281.5374.266. [PubMed] [CrossRef] [Google Scholar]
74. Иорданский С., Кашанчи Ф. Возможности радиационно-индуцированного клеточного стресса для реактивации латентного ВИЧ-1 и уничтожения инфицированных клеток. СПИД Рес Хум Ретровир
2016;32(2):120–4. 10.1089/АИД.2016.0006
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
75. Bruce JW, Ahlquist P, Young JA. Путь сульфирования клетки-хозяина способствует ретровирусной инфекции на этапе, совпадающем с установлением провируса. PLoS Патог
2008;4(11):e1000207. 10.1371/журнал.ppat.1000207. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
76. Коннор Р.И., Чен Б.К., Чоу С., Ландау Н.Р. Vpr необходим для эффективной репликации вируса иммунодефицита человека типа 1 в мононуклеарных фагоцитах. Вирусология
1995;206(2):935–44. 10.1006/viro.1995.1016. [PubMed] [CrossRef] [Google Scholar]
77. Becker JT, Sherer NM. Субклеточная локализация мРНК gag-pol ВИЧ-1 регулирует сайты сборки вириона. Дж Вирол. 2017;91(6). 10.1128/ОВИ.02315-16
Дж Вирол. 2017;91(6). 10.1128/ОВИ.02315-16
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
78. Ott M, Schnolzer M, Garnica J, Fischle W, Emiliani S, Rackwitz HR, et al. Ацетилирование белка Tat ВИЧ-1 с помощью p300 важно для его транскрипционной активности. Карр Биол
1999;9(24):1489–92. 10.1016/s0960-9822(00)80120-7 . [PubMed] [CrossRef] [Google Scholar]
79. Брюс Дж.В., Брэдли К.А., Алквист П., Янг Дж.А. Выделение клеточных линий, демонстрирующих новый, специфичный для вируса мышиного лейкоза, блокирующий ранние этапы репликации ретровируса. Джей Вирол
2005;79(20):12969–78. 10.1128/ОВИ.79.20.12969-12978.2005. [Статья бесплатно PMC] [PubMed] [CrossRef] [Google Scholar]
80. Chesebro B, Wehrly K, Nishio J, Perryman S. Изоляты макрофаготропного вируса иммунодефицита человека от разных пациентов демонстрируют необычную гомогенность последовательности оболочки V3 по сравнению с Т-клеточно-тропные изоляты: определение критических аминокислот, участвующих в клеточном тропизме. Джей Вирол
Джей Вирол
1992;66(11):6547–54. Эпб 1992/11/01. 10.1128/ОВИ.66.11.6547-6554.1992
[PMC free article] [PubMed] [CrossRef] [Google Scholar]
81. Нельсон Д.Д., Денисенко О., Бомштык К. Протокол метода быстрой иммунопреципитации хроматина (ChIP).
Нат Проток
2006;1(1):179–85. Эпб 2007/04/05. 10.1038/nprot.2006.27. [PubMed] [CrossRef] [Google Scholar]
82. Yandell BS. Практический анализ данных для запланированных экспериментов:
Чепмен и Холл; 1997. 440 с. [Google Scholar]
83. Koksal AS, Beck K, Cronin DR, McKenna A, Camp ND, Srivastava S, et al. Синтез сигнальных путей из временных фосфопротеомных данных. Cell Rep. 2018;24(13):3607–18. Эпублик 2018/09/27. 10.1016/j.celrep.2018.08.085
[Статья бесплатно PMC] [PubMed] [CrossRef] [Google Scholar]
Vpr ВИЧ-1 опосредует истощение клеточного репрессора CTIP2 для противодействия молчанию вирусных генов для борьбы с инфекциями. Млекопитающие выработали множество противовирусных факторов, таких как SAMHD1 или APOBEC3G, которые ограничивают экспрессию вируса
1,2,3 . Мы сообщали, что клеточный кофактор CTIP2 (Bcl11b) способствует установлению и сохранению латентного периода после интеграции ВИЧ-1 в клетках микроглии, основной мишени вируса в головном мозге 4,5,6 . CTIP2 работает как каркасный белок, рекрутируя по крайней мере два разных комплекса в клетках микроглии. Как часть комплекса ремоделирования хроматина, CTIP2 связан с лизиндеметилазой LSD1, гистондеацетилазами HDAC1 и HDAC2 и гистонметилтрансферазой SUV39h2 4,7,8,9 . В CD4+ Т-клетках CTIP2 ассоциирован с комплексом ремоделирования хроматина NuRD 10 . Помимо этого эпигенетического молчания, CTIP2 способствует контролю процесса элонгации транскрипции генов. Действительно, мы обнаружили, что CTIP2 связан с неактивным комплексом P-TEFb, включающим HEXIM1, HMGA1 и мяРНК 7SK 9.0412 11,12 . Как часть этого нового комплекса, CTIP2 подавляет функции P-TEFb и тем самым способствует ограничению реактивации латентно интегрированных провирусов ВИЧ-1. В целом, CTIP2 способствует установлению и сохранению латентности гена ВИЧ-1 в микроглиальных клетках, основных резервуарах вируса в центральной нервной системе.
Мы сообщали, что клеточный кофактор CTIP2 (Bcl11b) способствует установлению и сохранению латентного периода после интеграции ВИЧ-1 в клетках микроглии, основной мишени вируса в головном мозге 4,5,6 . CTIP2 работает как каркасный белок, рекрутируя по крайней мере два разных комплекса в клетках микроглии. Как часть комплекса ремоделирования хроматина, CTIP2 связан с лизиндеметилазой LSD1, гистондеацетилазами HDAC1 и HDAC2 и гистонметилтрансферазой SUV39h2 4,7,8,9 . В CD4+ Т-клетках CTIP2 ассоциирован с комплексом ремоделирования хроматина NuRD 10 . Помимо этого эпигенетического молчания, CTIP2 способствует контролю процесса элонгации транскрипции генов. Действительно, мы обнаружили, что CTIP2 связан с неактивным комплексом P-TEFb, включающим HEXIM1, HMGA1 и мяРНК 7SK 9.0412 11,12 . Как часть этого нового комплекса, CTIP2 подавляет функции P-TEFb и тем самым способствует ограничению реактивации латентно интегрированных провирусов ВИЧ-1. В целом, CTIP2 способствует установлению и сохранению латентности гена ВИЧ-1 в микроглиальных клетках, основных резервуарах вируса в центральной нервной системе.
Лентивирусы, такие как ВИО и ВИЧ, разработали несколько механизмов уклонения от врожденного и адаптивного иммунного ответа. Эти вирусы кодируют «вспомогательные» белки (Nef, Vif, Vpu, Vpx), которые позволяют уклоняться от иммунитета. Например, Vpx участвует в деградации SAMHD1 через протеасомный путь (обзор в 13 ). Деградация, опосредованная протеасомами, представляет собой привилегированный путь, нарушаемый ВИЧ-1 для противодействия клеточной защите. Связанный с убиквитинлигазным комплексом на основе Cul4A через DCAF1 (VprBP), дополнительный белок ВИЧ-1 Vpr, как давно предполагалось, нацеливается на еще не открытый фактор рестрикции хозяина для деградации, чтобы вызвать остановку G2 14,15 . Предполагается, что Vpr способствует деградации клеточных факторов, включая UNG2 16 , Dicer 17 , IRF3 18 , ZIP 19 , ДНК-транслоказу HTLF 20 и фактор пострепликационной репарации ДНК Exo1 21 . Путем активации комплекса SLX4 Vpr предотвращает соответствующий врожденный иммунный ответ 22 . Недавно было показано, что Vpr подавляет экспрессию ВИЧ-1 путем нацеливания на APOBEC3G 23 и еще не идентифицированный фактор рестрикции макрофагов 24 . Наконец, в двух недавних работах описывается, что человеческий комплекс сайленсинг-хаба (HUSH) также подвергается деградации с помощью Vpr и HIV-2/SIV Vpx 9.0412 25,26 . Интересно, что комплекс HUSH представлен авторами как мощный фактор рестрикции, регулирующий стадию транскрипции жизненного цикла вируса.
Недавно было показано, что Vpr подавляет экспрессию ВИЧ-1 путем нацеливания на APOBEC3G 23 и еще не идентифицированный фактор рестрикции макрофагов 24 . Наконец, в двух недавних работах описывается, что человеческий комплекс сайленсинг-хаба (HUSH) также подвергается деградации с помощью Vpr и HIV-2/SIV Vpx 9.0412 25,26 . Интересно, что комплекс HUSH представлен авторами как мощный фактор рестрикции, регулирующий стадию транскрипции жизненного цикла вируса.
Здесь мы показываем, что ВИЧ-1 разработал стратегию противодействия репрессии, опосредованной CTIP2. Мы сообщаем, что вирусный вспомогательный белок Vpr способствует деградации CTIP2 посредством физических и функциональных взаимодействий с комплексом Cul4A-DDB1-DCAF1. Vpr нацеливается на CTIP2, связанный с комплексом, модифицирующим гетерохроматин. Интересно, что экспрессия Vpr также коррелирует со сниженным связыванием CTIP2 на промоторе ВИЧ-1 и реактивацией латентного вируса в микроглиальной модели латентности CHME5-HIV.
Результаты
Экспрессия ВИЧ-1 способствует vpr-зависимой деградации ctip2
Чтобы исследовать возможную модуляцию экспрессии CTIP2 в ответ на инфекцию ВИЧ-1, мы измерили уровни его белка и его РНК во время экспериментов в Jurkat T -клетки и клетки микроглии.
После первоначальной индукции как мРНК CTIP2, так и экспрессии белка после первых 24 часов после заражения ВИЧ-1 (рис. 1, панели A и C) уровни экспрессии белка CTIP2 снизились в Т-клетках Jurkat (рис. 1B панель WT ) и в клетках микроглии (рис. 1D, панель WT) в более поздние моменты времени. Интересно, что хотя уровни мРНК CTIP2 не менялись с течением времени (от 24 часов до 9 часов).6 ч заражения), делеция гена Vpr (вирус с делецией Vpr — ΔVpr) отменяла истощение CTIP2 при экспрессии вируса (рис. 1B, D, панели ΔVpr). Чтобы подтвердить, что истощение CTIP2, опосредованное Vpr, происходит на посттранскрипционном этапе, мы затем сверхэкспрессировали CTIP2, помеченный FLAG, в присутствии нормализованных количеств провирусов WT и ΔVpr. Провирус WT-, но не ΔVpr, способствовал истощению CTIP2, экспрессируемого под контролем промотора CMV (рис. S1). Эти результаты подтвердили, что экспрессия CTIP2 подвергалась посттранскрипционному воздействию. Известно, что молекулы Vpr включаются в вирионы 27 . Чтобы определить, достаточно ли поступающих белков Vpr, чтобы вызвать истощение CTIP2 в первичных клетках, мы затем создали вирусоподобные частицы (VLP) для доставки Vpr в очищенные CD4+ Т-клетки. Как показано на рис. 2A, поступающий Vpr индуцировал значительное истощение CTIP2 в первичных CD4+ T-клетках, предполагая, что Vpr, продуцируемый в клетках при репликации ВИЧ-1, и Vpr, доставляемый вирионами при инфицировании, снижают экспрессию CTIP2. Поскольку было описано, что CTIP2 ограничивает реактивацию латентно интегрированных вирусов в клетки микроглии 9 , затем мы исследовали влияние входящего Vpr на модель микроглии CHME5-HIV латентности ВИЧ-1. Интересно, что доставка Vpr увеличила вдвое количество клеток, экспрессирующих ВИЧ-1 (рис.
Провирус WT-, но не ΔVpr, способствовал истощению CTIP2, экспрессируемого под контролем промотора CMV (рис. S1). Эти результаты подтвердили, что экспрессия CTIP2 подвергалась посттранскрипционному воздействию. Известно, что молекулы Vpr включаются в вирионы 27 . Чтобы определить, достаточно ли поступающих белков Vpr, чтобы вызвать истощение CTIP2 в первичных клетках, мы затем создали вирусоподобные частицы (VLP) для доставки Vpr в очищенные CD4+ Т-клетки. Как показано на рис. 2A, поступающий Vpr индуцировал значительное истощение CTIP2 в первичных CD4+ T-клетках, предполагая, что Vpr, продуцируемый в клетках при репликации ВИЧ-1, и Vpr, доставляемый вирионами при инфицировании, снижают экспрессию CTIP2. Поскольку было описано, что CTIP2 ограничивает реактивацию латентно интегрированных вирусов в клетки микроглии 9 , затем мы исследовали влияние входящего Vpr на модель микроглии CHME5-HIV латентности ВИЧ-1. Интересно, что доставка Vpr увеличила вдвое количество клеток, экспрессирующих ВИЧ-1 (рис. 2B). Эта величина реактивации была аналогична той, которая была получена при обработке TNFα (рис. 2B, столбец HA-Vpr по сравнению с TNFα). Поскольку ранее мы сообщали, что CTIP2 связывается со латентным промотором ВИЧ-1 в клетках микроглии, затем мы провели эксперименты с хроматином IP, нацеленные на CTIP2 в присутствии или без Vpr (рис. 2C). Как и ожидалось, было обнаружено, что CTIP2 связан с вирусным промотором, но не с геном люциферазы конструкции в клетках микроглии (рис. 2C: колонка IgG против (-) mock CTIP2 IP). Однако экспрессия Vpr значительно снижала связывание CTIP2 (рис. 2C: Vpr по сравнению с (-) имитацией) в соответствии с ранее наблюдаемым истощением белка в ядерных экстрактах. Было показано, что Vpr напрямую взаимодействует с протеасомой 26 S и разрушает клеточные факторы-мишени через протеасомный путь 28 . Мы действительно обнаружили, что CTIP2 связан с субъединицей 19S протеасомы, но не с Vpr (рис. S5). Чтобы дополнительно определить механизм, лежащий в основе истощения CTIP2, мы затем обработали клетки ингибитором протеасом MG132.
2B). Эта величина реактивации была аналогична той, которая была получена при обработке TNFα (рис. 2B, столбец HA-Vpr по сравнению с TNFα). Поскольку ранее мы сообщали, что CTIP2 связывается со латентным промотором ВИЧ-1 в клетках микроглии, затем мы провели эксперименты с хроматином IP, нацеленные на CTIP2 в присутствии или без Vpr (рис. 2C). Как и ожидалось, было обнаружено, что CTIP2 связан с вирусным промотором, но не с геном люциферазы конструкции в клетках микроглии (рис. 2C: колонка IgG против (-) mock CTIP2 IP). Однако экспрессия Vpr значительно снижала связывание CTIP2 (рис. 2C: Vpr по сравнению с (-) имитацией) в соответствии с ранее наблюдаемым истощением белка в ядерных экстрактах. Было показано, что Vpr напрямую взаимодействует с протеасомой 26 S и разрушает клеточные факторы-мишени через протеасомный путь 28 . Мы действительно обнаружили, что CTIP2 связан с субъединицей 19S протеасомы, но не с Vpr (рис. S5). Чтобы дополнительно определить механизм, лежащий в основе истощения CTIP2, мы затем обработали клетки ингибитором протеасом MG132. Как показано, обработка MG132 способствовала связыванию CTIP2 с вирусным промотором (MG132 по сравнению с (-) имитацией) и сильно ослабляла влияние Vpr (MG132+ Vpr по сравнению с MG132). В целом эти результаты свидетельствуют о том, что Vpr, образующийся в клетках при репликации ВИЧ-1, и частицы Vpr, включенные в вирионы, способствуют истощению CTIP2 в клеточных линиях и первичных клетках. Это истощение коррелирует со сниженным связыванием CTIP2 с вирусным промотором и реактивацией латентного ВИЧ-1. Кроме того, влияние MG132 на Vpr-опосредованное истощение CTIP2 и взаимодействие CTIP2 с 19S-субъединица протеасомы предполагает участие протеасомного пути и деградацию белка, а не регуляцию трансляции. Для дальнейшего биохимического исследования индуцированного Vpr истощения CTIP2 мы затем экспрессировали возрастающие количества Vpr в клетках, экспрессирующих CTIP2. Как и ожидалось, экспрессия Vpr способствовала дозозависимому истощению CTIP2 (рис. 3A). Следует отметить, что уровни мРНК CTIP2 в контроле и в клетках со сверхэкспрессией CTIP2 не подвергались значительному влиянию Vpr (рис.
Как показано, обработка MG132 способствовала связыванию CTIP2 с вирусным промотором (MG132 по сравнению с (-) имитацией) и сильно ослабляла влияние Vpr (MG132+ Vpr по сравнению с MG132). В целом эти результаты свидетельствуют о том, что Vpr, образующийся в клетках при репликации ВИЧ-1, и частицы Vpr, включенные в вирионы, способствуют истощению CTIP2 в клеточных линиях и первичных клетках. Это истощение коррелирует со сниженным связыванием CTIP2 с вирусным промотором и реактивацией латентного ВИЧ-1. Кроме того, влияние MG132 на Vpr-опосредованное истощение CTIP2 и взаимодействие CTIP2 с 19S-субъединица протеасомы предполагает участие протеасомного пути и деградацию белка, а не регуляцию трансляции. Для дальнейшего биохимического исследования индуцированного Vpr истощения CTIP2 мы затем экспрессировали возрастающие количества Vpr в клетках, экспрессирующих CTIP2. Как и ожидалось, экспрессия Vpr способствовала дозозависимому истощению CTIP2 (рис. 3A). Следует отметить, что уровни мРНК CTIP2 в контроле и в клетках со сверхэкспрессией CTIP2 не подвергались значительному влиянию Vpr (рис. 3B, C соответственно), что подтверждает посттранскрипционное влияние Vpr на экспрессию CTIP2. Для дальнейшего исследования участия протеасомного пути клетки микроглии обрабатывали ингибитором протеасом MG132. В соответствии с результатами ChIP, представленными на рис. 2C, MG132 повышал уровень эндогенной экспрессии CTIP2 в ядерных экстрактах (рис. 3D, ряд 7 и 5), что позволяет предположить, что физиологический оборот CTIP2 нуждается в функциональном протеасомном пути. Опять же, Vpr снижал экспрессию CTIP2 (рис. 3D, столбец 5 по сравнению с 1), а MG132 нарушал опосредованное Vpr истощение CTIP2 (рис. 3D, столбец 1 по сравнению с 3). Эти наблюдения убедительно свидетельствуют в пользу деградации CTIP2 протеасомным путем. Чтобы определить, происходит ли эта деградация в ядре, клетки обрабатывали лептомицином B (LMB), ингибитором ядерного экспорта. Как показано, обработка LMB существенно не влияла на уровень деградации CTIP2 под действием Vpr (рис. 3D, столбец 2 и 1). Затем мы воспользовались повторами этих экспериментов для количественной оценки влияния Vpr на уровни экспрессии CTIP2 в присутствии LMB и MG132.
3B, C соответственно), что подтверждает посттранскрипционное влияние Vpr на экспрессию CTIP2. Для дальнейшего исследования участия протеасомного пути клетки микроглии обрабатывали ингибитором протеасом MG132. В соответствии с результатами ChIP, представленными на рис. 2C, MG132 повышал уровень эндогенной экспрессии CTIP2 в ядерных экстрактах (рис. 3D, ряд 7 и 5), что позволяет предположить, что физиологический оборот CTIP2 нуждается в функциональном протеасомном пути. Опять же, Vpr снижал экспрессию CTIP2 (рис. 3D, столбец 5 по сравнению с 1), а MG132 нарушал опосредованное Vpr истощение CTIP2 (рис. 3D, столбец 1 по сравнению с 3). Эти наблюдения убедительно свидетельствуют в пользу деградации CTIP2 протеасомным путем. Чтобы определить, происходит ли эта деградация в ядре, клетки обрабатывали лептомицином B (LMB), ингибитором ядерного экспорта. Как показано, обработка LMB существенно не влияла на уровень деградации CTIP2 под действием Vpr (рис. 3D, столбец 2 и 1). Затем мы воспользовались повторами этих экспериментов для количественной оценки влияния Vpr на уровни экспрессии CTIP2 в присутствии LMB и MG132. Как показано на рис. 3E, Vpr способствовал более чем двукратному истощению CTIP2 в ядрах клеток микроглии (первая колонка). Однако MG132 устранял опосредованное Vpr истощение CTIP2 в присутствии или в отсутствие LMB (два последних столбца). В целом наши результаты свидетельствуют о том, что Vpr разрушает CTIP2 через протеасомный путь в ядрах клеток-мишеней ВИЧ-1.
Как показано на рис. 3E, Vpr способствовал более чем двукратному истощению CTIP2 в ядрах клеток микроглии (первая колонка). Однако MG132 устранял опосредованное Vpr истощение CTIP2 в присутствии или в отсутствие LMB (два последних столбца). В целом наши результаты свидетельствуют о том, что Vpr разрушает CTIP2 через протеасомный путь в ядрах клеток-мишеней ВИЧ-1.
Рисунок 1
Индуцированная CTIP2 экспрессия в инфицированных клетках противодействует ВИЧ-1 зависимым от Vpr образом. ( A , C ) Т-клетки Jurkat ( A ) и клетки микроглии ( C ) были инфицированы 25 × 10 3 копий/мл псевдотипированного провируса NL4.3ΔEnv-LUC VSV-G. 24 ч. Присутствие CTIP2 в инфицированных клетках оценивали с помощью вестерн-блоттинга, а мРНК CTIP2 определяли количественно с помощью RT-Q-PCR. ( B , D ) Т-клетки Jurkat ( B ) и клетки микроглии ( D ) инфицировали 150 × 10 3 копий/мл псевдотипированного VSV-G провируса NL4. 3ΔEnv-LUC (WT) и провируса NL4.3ΔEnvΔVpr-LUC (ΔVpr) для 24, 48 и 96 ч. Присутствие CTIP2 в инфицированных клетках оценивали с помощью вестерн-блоттинга, а экспрессию вируса определяли количественно с помощью люциферазного анализа. Количественные оценки представлены относительно количеств, полученных через 24 часа после заражения. Результаты являются репрезентативными как минимум для трех независимых экспериментов.
3ΔEnv-LUC (WT) и провируса NL4.3ΔEnvΔVpr-LUC (ΔVpr) для 24, 48 и 96 ч. Присутствие CTIP2 в инфицированных клетках оценивали с помощью вестерн-блоттинга, а экспрессию вируса определяли количественно с помощью люциферазного анализа. Количественные оценки представлены относительно количеств, полученных через 24 часа после заражения. Результаты являются репрезентативными как минимум для трех независимых экспериментов.
Изображение полного размера
Рисунок 2
Vpr способствует истощению CTIP2 в первичных CD4+ Т-клетках и на промоторе ВИЧ-1, вызывая реактивацию вируса в клетках микроглии. ( A ) Относительную экспрессию CTIP2 в Т-клетках CD4 количественно определяли с помощью проточной цитометрии. Уровни экспрессии в клетках, инкубированных с вирусоподобными частицами VLP-HA-Vpr, сравнивали с контрольными частицами VLP-HA, взятыми за 1. ( B ) Линию латентно инфицированных клеток микроглии CHME5-HIV инфицировали VPL или обрабатывали TNFα. Количество клеток GFP+ определяли количественно с помощью проточной цитометрии и представляли по отношению к клеткам GFP+, полученным после инфицирования VLP-HA. ( C ) Эксперименты по иммунопреципитации хроматина, нацеленные на эндогенный CTIP2 на промоторе ВИЧ-1, проводили с хроматином из микроглиальных клеток, экспрессирующих хроматинизированный эписомальный вектор LTR-LUC и Vpr, как указано. Клетки подвергали или не подвергали обработке MG132. Обогащение представлено в процентах от входов. В качестве контроля одновременно определяли присутствие CTIP2 в области гена люциферазы. Результаты являются репрезентативными по крайней мере для трех независимых экспериментов.
Количество клеток GFP+ определяли количественно с помощью проточной цитометрии и представляли по отношению к клеткам GFP+, полученным после инфицирования VLP-HA. ( C ) Эксперименты по иммунопреципитации хроматина, нацеленные на эндогенный CTIP2 на промоторе ВИЧ-1, проводили с хроматином из микроглиальных клеток, экспрессирующих хроматинизированный эписомальный вектор LTR-LUC и Vpr, как указано. Клетки подвергали или не подвергали обработке MG132. Обогащение представлено в процентах от входов. В качестве контроля одновременно определяли присутствие CTIP2 в области гена люциферазы. Результаты являются репрезентативными по крайней мере для трех независимых экспериментов.
Изображение в натуральную величину
Рисунок 3
Vpr нацеливает ядерный CTIP2 на деградацию посредством протеасомного пути. ( A ) Ядерные экстракты из клеток НЕК, экспрессирующих Tap-CTIP2 (t-CTIP2) и увеличивающееся количество GFP-Vpr (g-Vpr), анализировали с помощью вестерн-блоттинга на наличие указанных белков. ( B , C ) мРНК CTIP2 количественно определяли с помощью RT-Q-PCR в присутствии или без Vpr в отсутствие ( B ) и в присутствии ( C ) сверхэкспрессии CTIP2. Результаты представлены относительно контрольного вектора pCDNA3, взятого за один. ( D ) Экспрессию эндогенного CTIP2 анализировали вестерн-блоттингом в экстрактах клеток, экспрессирующих GFP-Vpr или контрольный GFP, и подвергали указанным обработкам. Клетки обрабатывали 10 нг/мл лептомицина В в течение 4 часов, а затем MG132 (5 мкг/мкл) в течение 6 часов перед лизисом и экстракцией ядерного белка. Экспрессию белка оценивали вестерн-блоттингом. ( E ) Экспрессия CTIP2 в присутствии GFP-Vpr была количественно определена по отношению к β-актину и представлена по отношению к количествам, полученным в присутствии контрольного белка GFP 9.0412 57 . Результаты являются репрезентативными по крайней мере для трех независимых экспериментов.
( B , C ) мРНК CTIP2 количественно определяли с помощью RT-Q-PCR в присутствии или без Vpr в отсутствие ( B ) и в присутствии ( C ) сверхэкспрессии CTIP2. Результаты представлены относительно контрольного вектора pCDNA3, взятого за один. ( D ) Экспрессию эндогенного CTIP2 анализировали вестерн-блоттингом в экстрактах клеток, экспрессирующих GFP-Vpr или контрольный GFP, и подвергали указанным обработкам. Клетки обрабатывали 10 нг/мл лептомицина В в течение 4 часов, а затем MG132 (5 мкг/мкл) в течение 6 часов перед лизисом и экстракцией ядерного белка. Экспрессию белка оценивали вестерн-блоттингом. ( E ) Экспрессия CTIP2 в присутствии GFP-Vpr была количественно определена по отношению к β-актину и представлена по отношению к количествам, полученным в присутствии контрольного белка GFP 9.0412 57 . Результаты являются репрезентативными по крайней мере для трех независимых экспериментов.
Изображение с полным размером
Ctip2 Взаимодействует с убиквитинлигазным комплексом cull4/ddb1-dcaf1
Сообщалось, что Vpr нацеливает клеточные белки на деградацию посредством рекрутирования комплекса Cul4A-DDB1-DCAF1. Поскольку ингибирование протеасомного пути увеличивает уровень экспрессии CTIP2 в отсутствие Vpr, мы сначала исследовали его возможное взаимодействие с убиквитинлигазным комплексом. Наблюдения с помощью конфокальной микроскопии проводились на клетках микроглии, экспрессирующих RFP-CTIP2, GFP-DCAF1 и HA-Vpr по отдельности (рис. 4A) или в комбинации (рис. 4B). Как описано ранее, CTIP2 локализован в доменах плотных и структурированных ядер 29 . Экспрессия HA-Vpr и GFP-DCAF1 в основном наблюдалась в ядерном компартменте. Однако комбинированная экспрессия RFP-CTIP2 с GFP-DCAF1 способствовала перемещению белков DCAF1 в структуры, индуцированные CTIP2 (рис. 4B, верхняя панель). Желтое окрашивание структур, индуцированных CTIP2, является результатом этого совместного расположения. Интересно, что экспрессия Vpr дополнительно окрашивала структуры CTIP2 в белый цвет, что свидетельствует о тройном совместном расположении Vpr, DCAF1 и CTIP2 (рис. 4B, нижняя панель). Ранее мы сообщали, что CTIP2 ассоциирован с Vpr в ядерных структурах, индуцированных CTIP2 7 .
Поскольку ингибирование протеасомного пути увеличивает уровень экспрессии CTIP2 в отсутствие Vpr, мы сначала исследовали его возможное взаимодействие с убиквитинлигазным комплексом. Наблюдения с помощью конфокальной микроскопии проводились на клетках микроглии, экспрессирующих RFP-CTIP2, GFP-DCAF1 и HA-Vpr по отдельности (рис. 4A) или в комбинации (рис. 4B). Как описано ранее, CTIP2 локализован в доменах плотных и структурированных ядер 29 . Экспрессия HA-Vpr и GFP-DCAF1 в основном наблюдалась в ядерном компартменте. Однако комбинированная экспрессия RFP-CTIP2 с GFP-DCAF1 способствовала перемещению белков DCAF1 в структуры, индуцированные CTIP2 (рис. 4B, верхняя панель). Желтое окрашивание структур, индуцированных CTIP2, является результатом этого совместного расположения. Интересно, что экспрессия Vpr дополнительно окрашивала структуры CTIP2 в белый цвет, что свидетельствует о тройном совместном расположении Vpr, DCAF1 и CTIP2 (рис. 4B, нижняя панель). Ранее мы сообщали, что CTIP2 ассоциирован с Vpr в ядерных структурах, индуцированных CTIP2 7 . Чтобы определить, взаимодействует ли CTIP2 напрямую с DCAF1, мы затем провели эксперименты по переносу энергии флуоресцентного резонанса (FRET). Как показано на рис. 4C, присутствие RFP-CTIP2 значительно снижает время жизни GFP-DCAF1 в ядерных структурах, что указывает на прямое взаимодействие между этими двумя белками. Удивительно, но присутствие Vpr не оказало существенного влияния на этот эффект. Чтобы биохимически подтвердить физическое взаимодействие между DCAF1 и CTIP2, мы провели эксперименты по совместной иммунопреципитации, нацеленные на первый CTIP2. DCAF1 и DDB1 были обнаружены в ассоциации с CTIP2 (рис. 4D). Эти ассоциации согласуются с повышенной экспрессией CTIP2, наблюдаемой после лечения MG132. Кроме того, мы обнаружили Vpr, связанный с CTIP2 и комплексом DDB1-DCAF1 в ядерных экстрактах из клеток, обработанных MG132 (рис. 4E). Эти результаты предполагают, что Vpr использует механизм клеточной деградации для истощения CTIP2 из клеток, инфицированных ВИЧ-1, и способствует экспрессии ВИЧ-1.
Чтобы определить, взаимодействует ли CTIP2 напрямую с DCAF1, мы затем провели эксперименты по переносу энергии флуоресцентного резонанса (FRET). Как показано на рис. 4C, присутствие RFP-CTIP2 значительно снижает время жизни GFP-DCAF1 в ядерных структурах, что указывает на прямое взаимодействие между этими двумя белками. Удивительно, но присутствие Vpr не оказало существенного влияния на этот эффект. Чтобы биохимически подтвердить физическое взаимодействие между DCAF1 и CTIP2, мы провели эксперименты по совместной иммунопреципитации, нацеленные на первый CTIP2. DCAF1 и DDB1 были обнаружены в ассоциации с CTIP2 (рис. 4D). Эти ассоциации согласуются с повышенной экспрессией CTIP2, наблюдаемой после лечения MG132. Кроме того, мы обнаружили Vpr, связанный с CTIP2 и комплексом DDB1-DCAF1 в ядерных экстрактах из клеток, обработанных MG132 (рис. 4E). Эти результаты предполагают, что Vpr использует механизм клеточной деградации для истощения CTIP2 из клеток, инфицированных ВИЧ-1, и способствует экспрессии ВИЧ-1.
Рисунок 4
CTIP2 взаимодействует с комплексом убиквитинлигазы Cull4-DDB1-DCAF1. ( A , B ) Клетки микроглии, экспрессирующие RFP-CTIP2, HA-Vpr и GFP-DCAF1 по отдельности (панель A) или в комбинации (панель B), подвергали конфокальной микроскопии. Масштабные полосы установлены на 5 мкм. ( C ) Время жизни из экспериментов FRET белков GFP представлено для каждого условия. Результаты являются репрезентативными для 5 независимых экспериментов и от 6 до 10 количественных определений для каждого условия на эксперимент. ( D , E ) Ядерные экстракты из клеток, экспрессирующих указанные белки, подвергали экспериментам по иммунопреципитации, нацеленным на Tap-CTIP2 (t-CTIP2) ( D ) и HA-Vpr ( E ). Исходные материалы и иммунопреципитированные комплексы анализировали с помощью вестерн-блоттинга. ( F ) Ядерные экстракты из клеток, экспрессирующих указанные белки, подвергали первой иммунопреципитации, направленной на FLAG-DCAF1 (f-DCAF), с антителами против FLAG. Комплексы, связанные с DCAF1, элюировали путем инкубации с пептидами FLAG и подвергали второй иммунопреципитации, нацеленной на CTIP2. Наличие указанных белков анализировали на каждом этапе методом вестерн-блоттинга.
Комплексы, связанные с DCAF1, элюировали путем инкубации с пептидами FLAG и подвергали второй иммунопреципитации, нацеленной на CTIP2. Наличие указанных белков анализировали на каждом этапе методом вестерн-блоттинга.
Изображение в полный размер
Мы сообщали, что CTIP2 связан с двумя разными и исключительными комплексами: комплексом, предназначенным для эпигенетического подавления экспрессии генов (ферменты, модифицирующие хроматин) 9 , и неактивной формой комплекса удлинения P-TEFb, включая 7SK мяРНК 11 . Чтобы охарактеризовать комплексы, содержащие DCAF1, связанные с CTIP2, мы провели последовательные эксперименты по иммунопреципитации (IP) (рис. 4F). В первом IP, нацеленном на DCAF1-ассоциированные комплексы, мы обнаружили CTIP2 и HDAC2 (фермент, модифицирующий хроматин), но не CDK9., субъединица киназы комплекса P-TEFb. Этот результат свидетельствует о том, что DCAF1 может взаимодействовать с CTIP2 и его комплексом, модифицирующим хроматин. Чтобы подтвердить, что CTIP2, HDAC2 и DCAF1 являются частью одного и того же комплекса, белки элюировали из первого IP и подвергали второму IP, нацеленному на CTIP2. Было обнаружено, что DCAF1 и HDAC2 связаны с CTIP2 в элюированном комплексе, содержащем DCAF1, что позволяет предположить, что CTIP2, DCAF1 и HDAC2 являются членами одного и того же комплекса (рис. 4F). В целом, эти результаты убедительно свидетельствуют о том, что DCAF1 взаимодействует и разрушает CTIP2, связанный с ферментным комплексом, модифицирующим хроматин (HDAC1/2, SUV39).h2), но не с CTIP2, связанным с неактивным комплексом P-TEFb. Этот вывод согласуется с деградацией HDAC1 под действием Vpr при заражении ВИЧ-1 (рисунок S3 и 30 ).
Было обнаружено, что DCAF1 и HDAC2 связаны с CTIP2 в элюированном комплексе, содержащем DCAF1, что позволяет предположить, что CTIP2, DCAF1 и HDAC2 являются членами одного и того же комплекса (рис. 4F). В целом, эти результаты убедительно свидетельствуют о том, что DCAF1 взаимодействует и разрушает CTIP2, связанный с ферментным комплексом, модифицирующим хроматин (HDAC1/2, SUV39).h2), но не с CTIP2, связанным с неактивным комплексом P-TEFb. Этот вывод согласуется с деградацией HDAC1 под действием Vpr при заражении ВИЧ-1 (рисунок S3 и 30 ).
Ассоциация с dcaf1 имеет решающее значение для опосредованной vpr деградации ctip2
Чтобы дополнительно охарактеризовать механистически деградацию CTIP2 под действием Vpr, мы исследовали, необходим ли DCAF1 для процесса опосредованной Vpr деградации, используя нокдаун на основе Si РНК. подход. Как и ожидалось, истощение DCAF1 отменяет деградацию CTIP2 (рис. 5A, столбец 4 и 2). Затем мы количественно определили уровни экспрессии CTIP2 в присутствии WT или мутированных белков Vpr (рис. 5B). Мутации Q65R (отменяющие связывание DCAF1 и остановку G2) и R80A (поддерживающие эффективное связывание DCAF1, но отменяющие остановку G2) были протестированы 14,31,32 . Как и ожидалось, CTIP2 практически не обнаруживался в присутствии белков Vpr WT и R80A (рис. 5B, столбцы 1 и 3). Однако мутация Q65R отменила Vpr-опосредованную деградацию CTIP2 (рис. 5B, столбец 2). Эти результаты продемонстрировали, что Vpr-опосредованная остановка G2 не влияет на экспрессию CTIP2, и подтвердили потребность в DCAF1 для истощения CTIP2 с помощью Vpr. Интересно, что при сильной сверхэкспрессии CTIP2, позволяющей обнаружить его в присутствии Vpr, мы смогли обнаружить белки Vpr WT, R80A и Q65R, связанные с CTIP2 (рис. 5C). Таким образом, наши результаты предполагают, что рекрутирование DCAF1 имеет решающее значение для обеспечения опосредованной Vpr деградации CTIP2, но необязательно для физических взаимодействий между белками.
5B). Мутации Q65R (отменяющие связывание DCAF1 и остановку G2) и R80A (поддерживающие эффективное связывание DCAF1, но отменяющие остановку G2) были протестированы 14,31,32 . Как и ожидалось, CTIP2 практически не обнаруживался в присутствии белков Vpr WT и R80A (рис. 5B, столбцы 1 и 3). Однако мутация Q65R отменила Vpr-опосредованную деградацию CTIP2 (рис. 5B, столбец 2). Эти результаты продемонстрировали, что Vpr-опосредованная остановка G2 не влияет на экспрессию CTIP2, и подтвердили потребность в DCAF1 для истощения CTIP2 с помощью Vpr. Интересно, что при сильной сверхэкспрессии CTIP2, позволяющей обнаружить его в присутствии Vpr, мы смогли обнаружить белки Vpr WT, R80A и Q65R, связанные с CTIP2 (рис. 5C). Таким образом, наши результаты предполагают, что рекрутирование DCAF1 имеет решающее значение для обеспечения опосредованной Vpr деградации CTIP2, но необязательно для физических взаимодействий между белками.
Рисунок 5
Связывание DCAF1 необходимо для Vpr-опосредованной деградации CTIP2. ( A ) Ядерные экстракты из контрольных клеток или клеток с нокдауном DCAF1 анализировали с помощью вестерн-блоттинга на наличие указанных белков в присутствии GFP-Vpr и контрольного GFP. Экспрессию CTIP2 количественно определяли относительно контроля загрузки с использованием программного обеспечения ImageJ. Показана эффективность нокдауна DCAF1 в наших экспериментах. ( B ) Ядерные экстракты из клеток, экспрессирующих указанные белки, анализировали с помощью вестерн-блоттинга. β-актин представлен в качестве контроля загрузки. ( C ) Ядерные экстракты из клеток, экспрессирующих большое количество Tap-CTIP2 (t-CTIP2) и указанные белки HA-Vpr, подвергали экспериментам по иммунопреципитации, направленным на метку HA. Вход и комплексы, связанные с Vpr, анализировали на наличие CTIP2 с помощью вестерн-блоттинга.
( A ) Ядерные экстракты из контрольных клеток или клеток с нокдауном DCAF1 анализировали с помощью вестерн-блоттинга на наличие указанных белков в присутствии GFP-Vpr и контрольного GFP. Экспрессию CTIP2 количественно определяли относительно контроля загрузки с использованием программного обеспечения ImageJ. Показана эффективность нокдауна DCAF1 в наших экспериментах. ( B ) Ядерные экстракты из клеток, экспрессирующих указанные белки, анализировали с помощью вестерн-блоттинга. β-актин представлен в качестве контроля загрузки. ( C ) Ядерные экстракты из клеток, экспрессирующих большое количество Tap-CTIP2 (t-CTIP2) и указанные белки HA-Vpr, подвергали экспериментам по иммунопреципитации, направленным на метку HA. Вход и комплексы, связанные с Vpr, анализировали на наличие CTIP2 с помощью вестерн-блоттинга.
Изображение полного размера
Обсуждение
CTIP2/Bcl11B участвует как в установлении, так и в сохранении латентного периода ВИЧ-1 в CD4+ Т-клетках и клетках микроглии 8,9,11,33 . Подавляя встроенные провирусы ВИЧ-1 и препятствуя их реактивации, этот клеточный кофактор представляет собой основной блок вирусной экспрессии. Для предотвращения абортивных инфекций ВИЧ-1 развил сложные механизмы уклонения от врожденного и адаптивного иммунного ответа. Дополнительные белки, такие как Nef, Vif, Vpu, Vpx и Vpr, связаны с некоторыми аспектами этого уклонения от иммунитета. Действительно, несколько факторов рестрикции нацелены на деградацию этими вспомогательными белками. Vif нацелен на APOBEC3G 23 , Vpu нацеливается на тетерин путем связывания с места почкования и протеасомной деградации 34,35 , а Vpx нацеливается на SAMHD1 2 . Среди так называемых вспомогательных белков, которые скорее следует рассматривать как ключевые факторы вирулентности, Vpr оставался загадочным. Vpr представляет собой небольшой белок (около 14 кДа), который участвует в нескольких биологических функциях, включая перенос в ядро прединтеграционного комплекса 36 ; экспрессия белка оболочки и продукция вириона 24 ; транскрипция ВИЧ-1 37 ; пострепликационная репарация ДНК 21 , сплайсинг гена ВИЧ-1 38 ; индукция апоптоза 39 и остановка клеточного цикла 22 (рассмотрено в 40 ).
Подавляя встроенные провирусы ВИЧ-1 и препятствуя их реактивации, этот клеточный кофактор представляет собой основной блок вирусной экспрессии. Для предотвращения абортивных инфекций ВИЧ-1 развил сложные механизмы уклонения от врожденного и адаптивного иммунного ответа. Дополнительные белки, такие как Nef, Vif, Vpu, Vpx и Vpr, связаны с некоторыми аспектами этого уклонения от иммунитета. Действительно, несколько факторов рестрикции нацелены на деградацию этими вспомогательными белками. Vif нацелен на APOBEC3G 23 , Vpu нацеливается на тетерин путем связывания с места почкования и протеасомной деградации 34,35 , а Vpx нацеливается на SAMHD1 2 . Среди так называемых вспомогательных белков, которые скорее следует рассматривать как ключевые факторы вирулентности, Vpr оставался загадочным. Vpr представляет собой небольшой белок (около 14 кДа), который участвует в нескольких биологических функциях, включая перенос в ядро прединтеграционного комплекса 36 ; экспрессия белка оболочки и продукция вириона 24 ; транскрипция ВИЧ-1 37 ; пострепликационная репарация ДНК 21 , сплайсинг гена ВИЧ-1 38 ; индукция апоптоза 39 и остановка клеточного цикла 22 (рассмотрено в 40 ). Vpr продуцируется при репликации ВИЧ-1, и значительное количество (275 молекул) включается в новый вирион 27 . Мы сообщаем здесь, что Vpr, экспрессируемый в инфицированных клетках (рис. 1), и поступающие молекулы Vpr (рис. 2) способствуют деградации CTIP2, как описано ранее для транслоказы HTLF 9.0412 20 . Интересно, что поступающий Vpr необходим для преодоления блока транскрипции HIV-1, наблюдаемого в дендритных клетках -41-. Влияние CTIP2 на дендритные клетки еще не изучено. Однако наши результаты показывают, что Vpr способствует разблокировке CTIP2-опосредованных блоков экспрессии гена ВИЧ-1. Было описано, что Vpr связан с убиквитинлигазным комплексом E3, который способствует опосредованной протеасомами деградации клеточных мишеней (для обзора 15 ). Здесь мы сообщаем, что CTIP2 взаимодействует с этим комплексом убиквитинлигазы через DCAF1/VprBP. Следует отметить, что DCAF1 взаимодействует и защищает Vpr от протеасомной деградации 42 .
Vpr продуцируется при репликации ВИЧ-1, и значительное количество (275 молекул) включается в новый вирион 27 . Мы сообщаем здесь, что Vpr, экспрессируемый в инфицированных клетках (рис. 1), и поступающие молекулы Vpr (рис. 2) способствуют деградации CTIP2, как описано ранее для транслоказы HTLF 9.0412 20 . Интересно, что поступающий Vpr необходим для преодоления блока транскрипции HIV-1, наблюдаемого в дендритных клетках -41-. Влияние CTIP2 на дендритные клетки еще не изучено. Однако наши результаты показывают, что Vpr способствует разблокировке CTIP2-опосредованных блоков экспрессии гена ВИЧ-1. Было описано, что Vpr связан с убиквитинлигазным комплексом E3, который способствует опосредованной протеасомами деградации клеточных мишеней (для обзора 15 ). Здесь мы сообщаем, что CTIP2 взаимодействует с этим комплексом убиквитинлигазы через DCAF1/VprBP. Следует отметить, что DCAF1 взаимодействует и защищает Vpr от протеасомной деградации 42 . Мы обнаружили, что Vpr, CTIP2 и DCAF1 совместно локализованы в плотных субъядерных структурах, а исследования FRET продемонстрировали прямую связь между CTIP2 и DCAF1. Эти наблюдения показали нам, что Vpr может разрушать протеасомный путь, чтобы способствовать деградации CTIP2. Интересно, что мы показали, что экспрессия белка CTIP2 выше в клетках, обработанных MG132, что свидетельствует о физиологической регуляции CTIP2 через протеасомный путь. Такая деградация белка CTIP2 была описана при физиологических состояниях, таких как активация TCR 9.0412 43,44 . Следовательно, Vpr способствует конститутивному DCAF1-зависимому обороту CTIP2. Такой механизм действия Vpr уже был описан для UNG2 16 и обсуждался в другом месте 15 . В соответствии с этим мы показываем, что Vpr усиливает убиквитинирование CTIP2 (рис. S2). Увеличение базального убиквитинирования уже описано для HDAC1 и HDAC3, белков, связанных с образованием гетерохроматина, компактно-неактивной формы промоторов 30,45 .
Мы обнаружили, что Vpr, CTIP2 и DCAF1 совместно локализованы в плотных субъядерных структурах, а исследования FRET продемонстрировали прямую связь между CTIP2 и DCAF1. Эти наблюдения показали нам, что Vpr может разрушать протеасомный путь, чтобы способствовать деградации CTIP2. Интересно, что мы показали, что экспрессия белка CTIP2 выше в клетках, обработанных MG132, что свидетельствует о физиологической регуляции CTIP2 через протеасомный путь. Такая деградация белка CTIP2 была описана при физиологических состояниях, таких как активация TCR 9.0412 43,44 . Следовательно, Vpr способствует конститутивному DCAF1-зависимому обороту CTIP2. Такой механизм действия Vpr уже был описан для UNG2 16 и обсуждался в другом месте 15 . В соответствии с этим мы показываем, что Vpr усиливает убиквитинирование CTIP2 (рис. S2). Увеличение базального убиквитинирования уже описано для HDAC1 и HDAC3, белков, связанных с образованием гетерохроматина, компактно-неактивной формы промоторов 30,45 . Далее мы сообщаем, что Vpr способствует деградации CTIP2 в ядре на промоторе ВИЧ-1. Это наблюдение убедительно доказывает косвенное влияние Vpr на транскрипцию гена ВИЧ-1. В результате деградации CTIP2 Vpr способствует преодолению подавления транскрипции, вызванного комплексами, связанными с CTIP2, и способствует функции Tat (рис. S4). Интересно, что мы обнаружили CTIP2, HDAC2 и DCAF1 в одном комплексе. Поскольку P-TEFb исключен из этого комплекса, наши результаты показывают, что Vpr способствует деградации CTIP2, связанной с HDAC1/2 и SUV39.ч2. Сопутствующая деградация CTIP2 и HDAC1 (рис. S3) и недавняя демонстрация того, что Vpr нацеливает HDAC1 на деградацию, опосредованную протеасомами, еще раз подтверждают эти выводы 30 . Более того, результаты недавнего скрининга факторов, на которые нацелены факторы вирулентности Vpr и HIV-2/SIV Vpx, подтверждают наши результаты 25,26 . Этот экран идентифицировал комплекс концентратора глушения человека (HUSH) как новую цель Vpr 46,47 .
Далее мы сообщаем, что Vpr способствует деградации CTIP2 в ядре на промоторе ВИЧ-1. Это наблюдение убедительно доказывает косвенное влияние Vpr на транскрипцию гена ВИЧ-1. В результате деградации CTIP2 Vpr способствует преодолению подавления транскрипции, вызванного комплексами, связанными с CTIP2, и способствует функции Tat (рис. S4). Интересно, что мы обнаружили CTIP2, HDAC2 и DCAF1 в одном комплексе. Поскольку P-TEFb исключен из этого комплекса, наши результаты показывают, что Vpr способствует деградации CTIP2, связанной с HDAC1/2 и SUV39.ч2. Сопутствующая деградация CTIP2 и HDAC1 (рис. S3) и недавняя демонстрация того, что Vpr нацеливает HDAC1 на деградацию, опосредованную протеасомами, еще раз подтверждают эти выводы 30 . Более того, результаты недавнего скрининга факторов, на которые нацелены факторы вирулентности Vpr и HIV-2/SIV Vpx, подтверждают наши результаты 25,26 . Этот экран идентифицировал комплекс концентратора глушения человека (HUSH) как новую цель Vpr 46,47 . Путем деградации CTIP2 и связанных с ним ферментов, стимулирующих гетерохроматин, Vpr разблокирует эпигенетический блок и активирует транскрипцию гена ВИЧ-1. Как прокомментировал 48 , наши результаты предполагают связь между врожденным иммунитетом и эпигенетическим контролем транскрипции гена ВИЧ-1, что может привести к новым способам борьбы с ВИЧ-1.
Путем деградации CTIP2 и связанных с ним ферментов, стимулирующих гетерохроматин, Vpr разблокирует эпигенетический блок и активирует транскрипцию гена ВИЧ-1. Как прокомментировал 48 , наши результаты предполагают связь между врожденным иммунитетом и эпигенетическим контролем транскрипции гена ВИЧ-1, что может привести к новым способам борьбы с ВИЧ-1.
В настоящее время имеется несколько доказательств того, что Vpr является ключевым фактором вирулентности. Было показано, что он нарушает несколько клеточных путей, включая остановку клеточного цикла (рассмотрено в 40 ) и репарацию ДНК (рассмотрено в 49 ). Участие Vpr в последнем пути было связано с ускользанием вируса от врожденного иммунного восприятия 22 . Мы и другие сообщили, что Vpr участвует в эпигенетической регуляции транскрипции гена ВИЧ-1. Vpr способствует деградации членов комплексов ремоделирования хроматина, таких как CTIP2, HDAC1 30, ZIP и sZIP, адаптеров комплекса NuRD 19. Интересно, что CTIP2 привлекает NuRD для подавления транскрипции гена ВИЧ-1 в CD4+ T-клетках 10 . Недавно мы показали, что PKC-опосредованное фосфорилирование Ser2 в CTIP2 отменяет рекрутирование NuRD при активации через TCR 9.0412 50 . Посттрансляционные модификации вызывают ассоциацию CTIP2 с различными комплексами и тем самым определяют функции CTIP2. Вопрос о том, способен ли Vpr различать различные формы CTIP2, требует дальнейшего изучения.
Интересно, что CTIP2 привлекает NuRD для подавления транскрипции гена ВИЧ-1 в CD4+ T-клетках 10 . Недавно мы показали, что PKC-опосредованное фосфорилирование Ser2 в CTIP2 отменяет рекрутирование NuRD при активации через TCR 9.0412 50 . Посттрансляционные модификации вызывают ассоциацию CTIP2 с различными комплексами и тем самым определяют функции CTIP2. Вопрос о том, способен ли Vpr различать различные формы CTIP2, требует дальнейшего изучения.
Распознавание функций Vpr в ускользании вируса от иммунного ответа в целом и в предотвращении латентности ВИЧ-1, как описано в настоящей статье, может иметь глубокие терапевтические последствия 51 . Недавно мы рассмотрели возможности нацеливания на комплексы репарации ДНК после репликации для предотвращения латентности ВИЧ-1 9.0412 52 . Использование Vpr-индуцированного истощения ключевых клеточных факторов может быть интересным вариантом, как недавно описано для пострепликационного белка репарации ДНК Exo1 21 .
Материалы и методы
Плазмиды
Большинство конструкций, используемых в наших анализах, были описаны ранее: pcDNA3, pNTAP, pFLAG-CTIP2 (f-CTIP2), pRFP-CTIP2, pNTAP-CTIP2 (t-CTIP2) 8,9,11 . pGFP-Vpr WT (g-Vpr), pNL- 4,3 ∆Env-luc дикого типа, pNL-4,3 ∆Env-luc ∆Vpr 19 и pMyc-DDB1 (m-DDB1), pFLAG-DCAF1 (f-DCAF1), pHA-Vpr wt, pHA-Vpr Q65R были любезно предоставлены доктором Ф. Марготен-Гогет.
Культура клеток
Человеческая микроглия (предоставлена M. Tardieu, Paris, France) 53 , клеточные линии HEK293T и CHME5-HIV поддерживали в модифицированной Дульбекко среде Игла (DMEM), а клеточную линию Jurkat — в RPMI 1640. культуральные среды дополняли 10% (об./об.) инактивированной нагреванием фетальной телячьей сыворотки (FBS) и 100 ЕД/мл пенициллина/стрептомицина. Там, где указано, клетки обрабатывали MG132 (5 мкг/мкл) в течение 6 часов, 10,0 нг/мл лептомицина B (LMB) в течение 5 часов перед сбором клеток.
Антитела и реагенты
Антитела CTIP2 (ab18465) были приобретены у Abcam, BCL11b (A300–384A) у Beethyl Laboratories, CDK9 (sc-8338), эпитоп Myc (9 E10), мышиный и крысиный HRP-конъюгированные у Santa Cruz Biotechnology, аффинный гель против FLAG M2 и β-актин (A5441) от Sigma-Aldrich, а антитело против HA. 11 Tag (AFC-101P) было от Eurogentec. Кроличьи HRP-конъюгированные антитела были приобретены у Thermo Fisher Scientific, анти-GFP (632592) у Clontech, а магнитные шарики с белком G у Millipore. Молекулы MG132 и лептомицина B были предоставлены Sigma-Aldrich, а смесь ингибиторов протеазы — Roche. VprBP (DCAF1) и нецелевые siРНК были получены от Dharmacon. Мастер-микс SYBR Select, используемый для Q-PCR, был получен от Thermo Fisher. CTIP2-FITC (25B6) ab123449и контроль IgG были приобретены у Abcam. Анти-HA.11-AF647 использовали для наблюдений с помощью конфокальной микроскопии.
11 Tag (AFC-101P) было от Eurogentec. Кроличьи HRP-конъюгированные антитела были приобретены у Thermo Fisher Scientific, анти-GFP (632592) у Clontech, а магнитные шарики с белком G у Millipore. Молекулы MG132 и лептомицина B были предоставлены Sigma-Aldrich, а смесь ингибиторов протеазы — Roche. VprBP (DCAF1) и нецелевые siРНК были получены от Dharmacon. Мастер-микс SYBR Select, используемый для Q-PCR, был получен от Thermo Fisher. CTIP2-FITC (25B6) ab123449и контроль IgG были приобретены у Abcam. Анти-HA.11-AF647 использовали для наблюдений с помощью конфокальной микроскопии.
Инфекции ВИЧ-1 и продукция вируса в клеточных линиях
Псевдотипированные вирусы VSV-G ΔEnv-LUC ВИЧ-1 были получены путем трансфекции pNL4.3 ΔEnv-LUC HIV-1 (WT) или pNL4.3 ΔEnvΔVpr-LUC ВИЧ-1 (ΔVpr) конструируется вместе с экспрессионной плазмидой VSV-G в 293 Т-клетках. Через 48 часов после трансфекции собирали культуральные супернатанты и измеряли продукцию вируса с помощью клинического теста на вирусную нагрузку ВИЧ-1 (количественное определение геномных РНК).
Экспрессия CTIP2 в первичных CD4+ T-клетках, инфицированных VLP
Первичные CD4+ T-клетки выделяли и очищали из мононуклеарных клеток периферической крови человека (PBMC) здоровых доноров путем положительной селекции с использованием наборов для селекции CD4 MicroBeads и сепаратора autoMACS Pro Separator (Miltenyi Biotec ) как описано ранее 54,55 . CD4 + Т-лимфоциты активировали фитогемаглютинином А (ФГА) (2 мкг/мл) (Sigma-Aldrich) в течение 3 дней в среде RPMI 1640 плюс среда Gibco GlutaMAX (Thermo Fisher) с добавлением 10% фетальной телячьей сыворотки (FCS). Клетки хранили замороженными. Их размораживали накануне использования. Т-клетки CD4 инкубировали с вирусоподобными частицами VLP-HA или VLP-HA-Vpr (полученными из FMG) в количестве 0,1 мкг на 0,1 миллиона клеток в течение 1 дня. Для количественной оценки внутриклеточной экспрессии CTIP2 клетки инкубировали в течение 10 мин при 4°С с молекулами клеточной поверхности CD3 перед фиксацией раствором Cytofix (BD Biosciences) и пермеабилизировали раствором 0,1% Triton X-100. CTIP2 или контрольный изотип IgG инкубировали в течение 30 мин при 4°С. После обширной промывки процент Т-клеток CD3-PEC, положительных в отношении экспрессии CTIP2, определяли с помощью проточной цитометрии (MACSQuant, Miltenyi) и анализировали с помощью программного обеспечения Kaluza.
CTIP2 или контрольный изотип IgG инкубировали в течение 30 мин при 4°С. После обширной промывки процент Т-клеток CD3-PEC, положительных в отношении экспрессии CTIP2, определяли с помощью проточной цитометрии (MACSQuant, Miltenyi) и анализировали с помощью программного обеспечения Kaluza.
Анализы ко-иммунопреципитации и Вестерн-блоттинг
Клетки, культивированные в чашках диаметром 150 мм, трансфицировали указанными плазмидами с использованием метода ко-преципитации с фосфатом кальция. Лизаты готовили через два дня после трансфекции, как описано ранее 11 . Иммунопреципитацию проводили по стандартной методике, как в 11 . Наконец, иммунопреципитированные комплексы обрабатывали для SDS-PAGE и иммуноблоттинга. Белки визуализировали методом хемилюминесценции с использованием системы обнаружения хемилюминесценции SuperSignal (Thermo Fisher).
Иммунопреципитация хроматина (ChIP)
Клетки, экспрессирующие хроматинизированную конструкцию эписомальной LTR-люциферазы ВИЧ-1, подвергали экспериментам ChIP с контрольным IgG или антителами IgG против CTIP2, как в 8,9 . Присутствие CTIP2 в областях промотора или гена люциферазы определяли количественно с помощью количественной ПЦР. Результаты представлены в процентах от входных данных. Значения являются репрезентативными для трех независимых экспериментов.
Присутствие CTIP2 в областях промотора или гена люциферазы определяли количественно с помощью количественной ПЦР. Результаты представлены в процентах от входных данных. Значения являются репрезентативными для трех независимых экспериментов.
Конфокальная микроскопия
Клетки микроглии трансфицировали в 24-луночные планшеты со стеклянным дном (Greiner Bio-One, Ref. 66289).2) со смесью ДНК, содержащей eGFP-DCAF1, mRFP-CTIP2 или HA-Vpr. Через 24 ч после трансфекции клетки тщательно промывали, фиксировали 4% раствором PFA/PBS и хранили в 1x PBS при 4°C до наблюдения с помощью конфокального микроскопа Leica SPE, оснащенного масляным иммерсионным объективом Leica 63×1.4NA (HXC PL). APO 63x/1.40 OIL CS).
Иммунофлуоресцентное окрашивание
Клетки микроглии, экспрессирующие HA-меченый Vpr, подвергали иммунодетекции, как описано ранее 56 . Анти-HA (BioLegend,

Флуоресцентная визуализирующая микроскопия времени жизни (FLIM)
Подсчет одиночных фотонов с временной корреляцией FLIM выполняли на самодельной лазерной сканирующей установке на основе инвертированного микроскопа Olympus IX70 с иммерсионным объективом Olympus 60×1,2NA в воде, как описан 56 . Двухфотонное возбуждение на длине волны 900 нм обеспечивалось лазером InSight DeepSee (Spectra Physics). Для FLIM мощность лазера была отрегулирована таким образом, чтобы обеспечить скорость счета с пиками до 10 6 фотонов с −1 , так что эффектом наложения можно пренебречь. Фотоны собирались с помощью короткопропускающего фильтра с длиной волны отсечки 680 нм (F75-680, AHF, Германия) и полосового фильтра 520 ± 17 нм (F37-520, AHF, Германия). Флуоресценция направлялась на АФД с волоконной связью (SPCM-AQR-14-FC, Perkin Elmer), который был подключен к модулю счета одиночных фотонов с временной корреляцией (SPC83, Becker and Hickl, Германия). Как правило, образцы непрерывно сканировали в течение примерно 60 с, чтобы получить соответствующую статистику фотонов для анализа затухания флуоресценции. Явление FRET вызывает уменьшение времени жизни флуоресценции (τ) донора, которое можно измерить методом FLIM для каждого пикселя или группы пикселей. Эксперименты проводились с eGFP в качестве донора FRET и mRFP в качестве акцептора. Эффективность FRET (E) рассчитывали по формуле: E = 1 − τ DA /τ D = 1/1 + (R/R 0 ) 6 где τ DA – время жизни донора в присутствии акцептора, а τ D – время жизни донора в присутствии акцептора. донора в отсутствие акцептора. Расстояние Förster R 0 (где эффективность переноса составляет 50%), равное 56 Ä, было рассчитано между eGFP, используемым в качестве донора, и mRFP, используемым в качестве акцептора.
Явление FRET вызывает уменьшение времени жизни флуоресценции (τ) донора, которое можно измерить методом FLIM для каждого пикселя или группы пикселей. Эксперименты проводились с eGFP в качестве донора FRET и mRFP в качестве акцептора. Эффективность FRET (E) рассчитывали по формуле: E = 1 − τ DA /τ D = 1/1 + (R/R 0 ) 6 где τ DA – время жизни донора в присутствии акцептора, а τ D – время жизни донора в присутствии акцептора. донора в отсутствие акцептора. Расстояние Förster R 0 (где эффективность переноса составляет 50%), равное 56 Ä, было рассчитано между eGFP, используемым в качестве донора, и mRFP, используемым в качестве акцептора.
Анализы люциферазы
Клетки микроглии, культивированные в 48-луночных планшетах, трансфицировали указанными векторами и контрольным вектором люциферазы CMV-Renilla с использованием метода соосаждения с фосфатом кальция. Два дня спустя клетки собирали и определяли активность люциферазы светлячка с использованием системы анализа люциферазы Dual-Glo (Promega, Мэдисон, Висконсин, США) и нормализовали по активности люциферазы Renilla. Значения соответствуют среднему значению по меньшей мере трех независимых экспериментов, проведенных в трех повторностях.
Значения соответствуют среднему значению по меньшей мере трех независимых экспериментов, проведенных в трех повторностях.
Количественное определение мРНК
Суммарную РНК экстрагировали с использованием мини-набора RNeasy Plus (Qiagen, Джермантаун, Мэриленд, США) в соответствии с инструкциями производителя. Используя обратную транскриптазу SuperScript III (Thermo Fisher) и олиго(dT)12–18 праймеров (Thermo Fisher), РНК подвергали обратной транскрипции в кДНК. кДНК разводили в 10 раз водой без ДНКазы. Количественную ПЦР проводили на разбавленной кДНК с использованием SYBR Select Master Mix. Праймеры, используемые в количественной ПЦР, включают: CTIP2-F 5′-ATTGGAACCTGCCACTTG-3′, CTIP2-R 5′-TTTGCCTGTGTTCCACGA-3′ GAPDH-F5′-GAGAAGGCTGGGGCTCATTT-3′, GAPDH-R 5′-GCAGTGATGGCATGGACTGT-3′. Данные были нормализованы к GAPDH и рассчитаны с использованием 2 — (ΔΔCT) метод.
Статистический анализ
Данные были подвергнуты статистическому анализу с использованием тестов t в программах Excel (Microsoft) или StatView (SAS Institute Inc. ). Значение p < 0,05 считалось статистически значимым. Результаты выражали как S.D. и представляют данные как минимум из трех независимых экспериментов.
). Значение p < 0,05 считалось статистически значимым. Результаты выражали как S.D. и представляют данные как минимум из трех независимых экспериментов.
Ссылки
Descours, B. и др. . SAMHD1 ограничивает обратную транскрипцию ВИЧ-1 в покоящихся CD4(+) Т-клетках. Ретровирусология 9 , 87 (2012).
Артикул
КАСGoogle Scholar
Лагетт, Н. и др. . SAMHD1 представляет собой рестрикционный фактор ВИЧ-1, специфичный для дендритных и миелоидных клеток, которому противодействует Vpx. Природа 474 , 654–7 (2011).
Артикул
КАСGoogle Scholar
Лахуасса, Х. и др. . SAMHD1 ограничивает репликацию вируса иммунодефицита человека типа 1, истощая внутриклеточный пул дезоксинуклеозидтрифосфатов.
 Нац. Иммунол. 13 , 223–8 (2012).
Нац. Иммунол. 13 , 223–8 (2012).Артикул
КАСGoogle Scholar
Ле Дус, В., Шеррье, Т., Рикле, Р., Рор, О. и Шварц, К. Многочисленные жизни CTIP2: от СПИДа до рака и сердечной гипертрофии. Дж. Сотовый. Физиол. 229 , 533–537 (2014).
Артикул
Google Scholar
Ле Дус, в. и др. . HIC1 контролирует транскрипцию клеточных генов и генов ВИЧ-1 посредством взаимодействия с CTIP2 и HMGA1. науч. 6 , 34920 (2016).
Артикул
ОБЪЯВЛЕНИЯGoogle Scholar
Марбан, К. и др. . Ориентация на резервуары мозга: на пути к излечению от ВИЧ. Фронт. Иммунол. 7 , 397 (2016).
Артикул
Google Scholar
«>Ле Дус, В. и др. . LSD1 взаимодействует с CTIP2, чтобы способствовать подавлению транскрипции ВИЧ-1. Рез. нуклеиновых кислот. 40 , 1904–15 (2012).
Артикул
Google Scholar
Марбан, К. и др. . Рекрутирование ферментов, модифицирующих хроматин, с помощью CTIP2 способствует подавлению транскрипции ВИЧ-1. Embo J 26 , 412–423 (2007).
Артикул
КАСGoogle Scholar
Чишмасиу В.Б. и др. . BCL11B функционально связывается с комплексом NuRD в Т-лимфоцитах для репрессии целевого промотора.
 Онкоген 24 , 6753–6764 (2005).
Онкоген 24 , 6753–6764 (2005).Артикул
КАСGoogle Scholar
Черриер, Т. и др. . CTIP2 является негативным регулятором P-TEFb. Proc Natl Acad Sci USA 110 , 12655–60 (2013).
Артикул
ОБЪЯВЛЕНИЯ
КАСGoogle Scholar
Эйлебрехт, С. и др. . HMGA1 рекрутирует CTIP2-репрессированный P-TEFb к промоторам ВИЧ-1 и клеточным мишеням. Рез. нуклеиновых кислот. 42 , 4962–71 (2014).
Артикул
КАСGoogle Scholar
Машиба, М. и Коллинз, К.Л. Молекулярные механизмы уклонения ВИЧ от врожденного иммунного ответа в миелоидных клетках. Вирусы 5 , 1–14 (2013).
Артикул
КАСGoogle Scholar
«>Romani, B. & Cohen, E.A. Дополнительные белки лентивирусов Vpr и Vpx узурпируют убиквитинлигазу E3 cullin4-DDB1 (DCAF1). Курс. мнение Вирол. 2 , 755–63 (2012).
Артикул
КАСGoogle Scholar
Wen, X., Casey Klockow, L., Nekorchuk, M., Sharifi, HJ, & de Noronha, C.M.C. Белок ВИЧ1 Vpr действует, усиливая конститутивный DCAF1-зависимый оборот UNG2. PLoS One 7 , e30939 (2012 г.).
Артикул
ОБЪЯВЛЕНИЯ
КАСGoogle Scholar
Кейси Клокоу, Л. и др. . Белок ВИЧ-1 Vpr нацеливается на эндорибонуклеазу Dicer для протеасомной деградации, чтобы усилить инфекцию макрофагов.
 Вирусология 444 , 191–202 (2013).
Вирусология 444 , 191–202 (2013).Артикул
КАСGoogle Scholar
Окумура, А. и др. . Дополнительные белки ВИЧ-1 VPR и Vif модулируют противовирусный ответ, направляя IRF-3 для деградации. Вирусология 373 , 85–97 (2008).
Артикул
КАСGoogle Scholar
Моде, К. и др. . Vpr ВИЧ-1 индуцирует деградацию ZIP и sZIP, адаптеров комплекса ремоделирования хроматина NuRD, путем захвата DCAF1/VprBP. PLoS One 8 , e77320 (2013 г.).
Артикул
ОБЪЯВЛЕНИЯ
КАСGoogle Scholar
Лахуасса, Х. и др. . Vpr ВИЧ-1 разрушает транслоказу ДНК HLTF в Т-клетках и макрофагах. Проц. Натл. акад. науч. США 113 , 5311–6 (2016).
Артикул
ОБЪЯВЛЕНИЯ
КАСGoogle Scholar
«>Лагетт, Н. и др. . Преждевременная активация комплекса SLX4 с помощью Vpr способствует аресту G2/M и ускользанию от врожденного иммунного восприятия. Ячейка 156 , 134–45 (2014).
Артикул
КАСGoogle Scholar
Чжоу, Д. и др. . Дополнительный белок ВИЧ-1 Vpr индуцирует деградацию анти-ВИЧ-1 агента APOBEC3G посредством протеасомного пути, опосредованного VprBP. Virus Res ., https://doi.org/10.1016/j.virusres.2014.08.021 (2014).
Артикул
КАСGoogle Scholar
Машиба, М., Коллинз, Д. Р., Терри, В. Х. и Коллинз, К. Л. Vpr преодолевает специфичное для макрофагов ограничение экспрессии Env ВИЧ-1 и продукции вириона.
 Микроб-хозяин клетки 16 , 722–35 (2014).
Микроб-хозяин клетки 16 , 722–35 (2014).Артикул
КАСGoogle Scholar
Юрковецкий Л. и др. . Белки вируса иммунодефицита приматов Vpx и Vpr противодействуют репрессии транскрипции провирусов комплексом HUSH. Нац. Микробиол ., https://doi.org/10.1038/s41564-018-0256-x (2018).
Артикул
КАСGoogle Scholar
Чоуги, Г. и др. . Вирусный белок X ВИЧ-2/SIV противодействует репрессорному комплексу HUSH. Нац. микробиол. 3 , 891–897 (2018).
Артикул
КАСGoogle Scholar
Müller, B., Tessmer, U., Schubert, U. & Kräusslich, H.G. Белок Vpr вируса иммунодефицита человека типа 1 включается в вирион в значительно меньших количествах, чем gag, и фосфорилируется в инфицированных клетках.
 Дж. Вирол. 74 , 9727–9731 (2000).
Дж. Вирол. 74 , 9727–9731 (2000).Артикул
Google Scholar
Ли, Г. и др. . Репликация ВИЧ-1 через hHR23A-опосредованное взаимодействие Vpr с протеасомой 26S. PLoS One 5 , e11371 (2010 г.).
Артикул
ОБЪЯВЛЕНИЯGoogle Scholar
Рор, О. и др. . Рекрутирование Tat к белку гетерохроматина HP1 посредством взаимодействия с CTIP2 ингибирует репликацию вируса иммунодефицита человека типа 1 в клетках микроглии. J Virol 77 , 5415–5427 (2003).
Артикул
КАСGoogle Scholar
Романи, Б., Байглу, Н.С., Хамиди-Фард, М., Агасадеги, М.Р. и Аллахбахши, Э. Белок ВИЧ-1 Vpr индуцирует протеасомную деградацию ассоциированных с хроматином HDAC класса I для преодоления латентной инфекции макрофагов.
 Дж. Биол. хим. 291 , 2696–711 (2016).
Дж. Биол. хим. 291 , 2696–711 (2016).Артикул
КАСGoogle Scholar
ДеХарт, Дж. Л. и др. . Vpr ВИЧ-1 активирует контрольную точку G2 посредством манипуляций с убиквитиновой протеасомной системой. Вирол. J. 4 , 57 (2007).
Артикул
Google Scholar
Lv, L. и др. . Vpr нацеливается на TET2 для деградации лигазой CRL4 VprBP E3 для поддержания экспрессии IL-6 и усиления репликации ВИЧ-1. Мол. Сотовый 70 , 961–970.e5 (2018).
Артикул
КАСGoogle Scholar
Чишмасиу, В. Б. и др. . BCL11B является общим репрессором транскрипции длинного концевого повтора ВИЧ-1 в Т-лимфоцитах посредством рекрутирования комплекса NuRD. Вирусология 380 , 173–181 (2008).

Артикул
КАСGoogle Scholar
Митчелл, Р. С. и др. . Vpu противодействует BST-2-опосредованному ограничению высвобождения ВИЧ-1 через бета-TrCP и эндолизосомальный перенос. PLoS Pathog. 5 , e1000450 (2009 г.).
Артикул
Google Scholar
Дуглас, Дж. Л. и др. . Vpu направляет деградацию фактора рестрикции вируса иммунодефицита человека BST-2/тетерина посредством {beta}TrCP-зависимого механизма. Дж. Вирол. 83 , 7931–47 (2009).
Артикул
КАСGoogle Scholar
Попов С. и др. . Вирусный белок R регулирует ядерный импорт преинтеграционного комплекса ВИЧ-1. EMBO J. 17 , 909–17 (1998).
Артикул
КАСGoogle Scholar
«>Курамицу, М. и др. . Новая роль Vpr вируса иммунодефицита человека типа 1 в качестве регулятора сплайсинга клеточной пре-мРНК. Заражение микробами. 7 , 1150–60 (2005).
Артикул
КАСGoogle Scholar
Nishizawa, M., Kamata, M., Mojin, T., Nakai, Y. & Aida, Y. Индукция апоптоза белком Vpr вируса иммунодефицита человека типа 1 происходит независимо от G(2) ареста клеточный цикл. Вирусология 276 , 16–26 (2000).
Артикул
КАСGoogle Scholar
«>Миллер, К.М. и др. . Вирион-ассоциированный Vpr ослабляет постинтеграционный блок в отношении инфицирования дендритных клеток ВИЧ-1. Дж. Вирол. 91 , e00051–17 (2017).
ПабМед
ПабМед ЦентральныйGoogle Scholar
Ле Рузик, Э. и др. . Сборка с убиквитинлигазой Cul4A-DDB1 DCAF1 защищает Vpr ВИЧ-1 от протеасомной деградации. Дж. Биол. хим. 283 , 21686–21692 (2008 г.).
Артикул
Google Scholar
Чжан, Л. и др. . Координированная регуляция активности фактора транскрипции Bcl11b в тимоцитах с помощью путей митоген-активируемой протеинкиназы (MAPK) и сумоилирования белка.
 Дж. Биол. хим. 287 , 26971–26988 (2012).
Дж. Биол. хим. 287 , 26971–26988 (2012).Артикул
КАСGoogle Scholar
Selman, W. H., Esfandiari, E. & Filtz, TM. Изменение Bcl11b при стимуляции как MAP-киназы, так и Gsk3-зависимых сигнальных путей в дважды отрицательных тимоцитах. Биохим. Клеточная биол. 97 , 201–213 (2019).
Артикул
КАСGoogle Scholar
Романи, Б. и др. . Vpr ВИЧ-1 реактивирует латентный провирус ВИЧ-1, вызывая истощение HDAC класса I на хроматине. науч. Респ. 6 , 31924 (2016).
Артикул
ОБЪЯВЛЕНИЯ
КАСGoogle Scholar
Роббез-Массон, ул. и др. . Комплекс HUSH взаимодействует с TRIM28 для репрессии молодых ретротранспозонов и новых генов. Рез. генома. 28 , 836–845 (2018).

Артикул
КАСGoogle Scholar
Часовникарова И. А. и др. . Эпигенетическое молчание с помощью комплекса HUSH опосредует пестроту эффектов положения в клетках человека. Наука (80-.). 348 , 1481–1485 (2015).
Артикул
ОБЪЯВЛЕНИЯ
КАСGoogle Scholar
Ван Линт, К. Хватит замалчивать SIV/ВИЧ. Нац. микробиол. 3 , 1336–1338 (2018).
Артикул
Google Scholar
Brégnard, C., Benkirane, M. & Laguette, N. Механизм восстановления повреждений ДНК и ускользание ВИЧ от врожденного иммунного восприятия. Фронт. микробиол. 5 , 176 (2014).
ПабМед
ПабМед ЦентральныйGoogle Scholar
Дюбюисез, М.
 и др. . Опосредованное протеинкиназой С фосфорилирование BCL11B по серину 2 отрицательно регулирует его взаимодействие с комплексами NuRD во время активации CD4+ Т-клеток. Мол. Клетка. биол. 36 , 1881–98 (2016).
и др. . Опосредованное протеинкиназой С фосфорилирование BCL11B по серину 2 отрицательно регулирует его взаимодействие с комплексами NuRD во время активации CD4+ Т-клеток. Мол. Клетка. биол. 36 , 1881–98 (2016).Артикул
Google Scholar
Шварц, К. и др. . На пути к излечению: очистка латентных резервуаров ВИЧ-1. Биохим. Фармакол ., https://doi.org/10.1016/j.bcp.2017.07.001 (2017).
Артикул
КАСGoogle Scholar
Schwartz, C., Rohr, O. & Wallet, C. Ориентация на комплекс ДНК-PK: его рациональное использование при раке и ВИЧ-1-инфекции. Биохим. Фармакол. https://doi.org/10.1016/J.BCP.2018.12.002 (2018 г.).
Артикул
пабмедGoogle Scholar
Джанаби, Н., Педенье, С., Герон, Б., Нг, К.
 Х. и Тардье, М. Создание линий клеток микроглии человека после трансфекции первичных культур эмбриональных клеток микроглии большим Т-антигеном SV40. Неврологи. лат. 195 , 105–108 (1995).
Х. и Тардье, М. Создание линий клеток микроглии человека после трансфекции первичных культур эмбриональных клеток микроглии большим Т-антигеном SV40. Неврологи. лат. 195 , 105–108 (1995).Артикул
КАСGoogle Scholar
Вс, Б. и др. . Нейтрализующие антитела ингибируют перенос ВИЧ-1 от первичных дендритных клеток к аутологичным CD4 Т-лимфоцитам. Кровь 120 , 3708–3717 (2012).
Артикул
КАСGoogle Scholar
Холл, В. и др. . Стимуляция репликации ВИЧ-1 в незрелых дендритных клетках в контакте с первичными CD4 Т- или В-лимфоцитами. Дж. Вирол. 84 , 4172–4182 (2010).
Артикул
КАСGoogle Scholar
Fritz, J. V. и др. . Прямое взаимодействие Vpr-Vpr в клетках отслеживается с помощью двухфотонной флуоресцентной корреляционной спектроскопии и визуализации времени жизни флуоресценции.
 Ретровирусология 5 , 87 (2008).
Ретровирусология 5 , 87 (2008).Артикул
Google Scholar
McDonald, D., Carrero, G., Andrin, C., de Vries, G. & Hendzel, M.J. Нуклеоплазматический бета-актин существует в динамическом равновесии между малоподвижными полимерными видами и быстро диффундирующими популяциями. J. Cell Biol. 172 , 541–52 (2006).
Артикул
КАСGoogle Scholar
Черриер, Т. и др. . Промотор гена p21(WAF1) эпигенетически замалчивается с помощью CTIP2 и SUV39h2. Онкоген 28 , 3380–9 (2009).
Артикул
КАС
Google Scholar
Ле Рузик, Э. и др. . Vpr ВИЧ1 останавливает клеточный цикл, рекрутируя DCAF1/VprBP, рецептор убиквитинлигазы Cul4-DDB1. Cell Cycle 6 , 182–8 (2007).
Артикул
Google Scholar
Ян Дж. и др. . Vpr ВИЧ-1 перепрограммирует CLR4 DCAF1 E3 Убиквитинлигаза для противодействия опосредованному экзонуклеазой 1 ограничению инфекции ВИЧ-1. МБио 9 (2018).
Кино, Т. и др. . Дополнительный белок Vpr вируса иммунодефицита человека типа 1 (ВИЧ-1) индуцирует транскрипцию промоторов, реагирующих на ВИЧ-1 и глюкокортикоиды, путем непосредственного связывания с коактиваторами p300/CBP. Дж. Вирол. 76 , 9724–34 (2002).
Артикул
КАС
Google Scholar
Guenzel, C. A., Hérate, C. & Benichou, S. HIV-1 Vpr — все еще «загадочный многозадачный человек». Фронт. микробиол. 5 , 127 (2014).
Артикул
Google Scholar
Скачать ссылки
Благодарности
Мы благодарны Андреа Яносси за внимательное и критическое прочтение рукописи, а также Джеймсу Хатчинсу за исправление научного английского языка. Работа в операционной лаборатории поддерживалась грантами Французского агентства по изучению СПИДа и вирусных гепатитов (ARNS), Sidaction, исследовательской и инновационной программы Европейского Союза Horizon 2020 по соглашению о гранте № 6 — EU4HIVCURE — h3020-MSCA-RISE- 2015 г. , Эльзас по борьбе с раком, Университетский институт Франции и Страсбургский университет.
, Эльзас по борьбе с раком, Университетский институт Франции и Страсбургский университет.
Информация об авторе
Авторы и организации
Страсбургский университет, EA7292, FMTS, IUT Louis Pasteur, Schiltigheim, France
F. Forouzanfar, S. Ali, C. De Wallet, M.H. Мекдад, М. Эль Маассарани, А. Айт-Аммар, Дж. Ван Аше, Ф. Дауад, К. Шварц и О. Рор
Институт микробиологии Сельскохозяйственного университета, Фейсалабад, Пакистан
С. Али
INSERM U1109, Fédération de Médecine Translationnelle (FMTS), Страсбургский университет, Страсбург, Франция
C. Ducloy & C. Moog
Université de Strasbourg, UMR 7021 CNRS, Illkirch, France
E. Boutant
Инсайс.
F. Margottin-goguet
CNRS, UMR8104, Paris, France
F. Margottin-goguet
Université Paris Decartes, Sorbonne Paris, Paris, France
F. Maretin-Gogtin-Gogtin-Gogtin-Gogtin-Gogtin-Gogtin-Gogtin-Gogtin-Gogtin-Gogtin-Gogtin-Gogtin-Gogtin.
 0021
0021Свободный университет Брюсселя (ULB), Служба молекулярной вирусологии, кафедра молекулярной биологии (DBM), Госселис, Бельгия
A. Aït-Ammar и C. Van Lint
- Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - S. Ali
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Академия - C. Бумажник
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - M. De Rovere
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - C. Ducloy
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - Х. Эль-Мекдад
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - M.
 El Maassarani
El MaassaraniПросмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - A. Aït-Ammar
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - J. Van Assche
Посмотреть публикации автора
Вы также можете искать этого автора в
PubMed Google Scholar - E. Boutant
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - F. Daouad
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - F. Margottin-Goguet
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Академия - C. Moog
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - C.
 Van Lint
Van LintПросмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - C. Schwartz
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - О. Рор
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar
9003 Авторы
1 F.
Вклады
F.F., A.S., DRM, DC, E.H., E.M.M., D.F., V.A.J. и У.К. проводили опыты. A.A.A., B.E., M.C. и М.Г.Ф. предоставлены технические ресурсы, научные и технические знания. В.Л.К., С.К. и Р.О. разработал и руководил экспериментами, написал проект и предоставил средства.
Авторы, переписывающиеся
Соответствие
К. Ван Линт, К. Шварц или О. Рор.
Декларации этики
Конкурирующие интересы
Авторы не заявляют о конкурирующих интересах.
Дополнительная информация
Примечание издателя: Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности.
Дополнительная информация
Дополнительная информация
Права и разрешения
Открытый доступ Эта статья находится под лицензией Creative Commons Attribution 4.0 International License, которая разрешает использование, совместное использование, адаптацию, распространение и воспроизведение на любом носителе или в любом формате при условии, что вы укажете автора(ов) оригинала. и источник, предоставьте ссылку на лицензию Creative Commons и укажите, были ли внесены изменения. Изображения или другие сторонние материалы в этой статье включены в лицензию Creative Commons для статьи, если иное не указано в кредитной строке материала. Если материал не включен в лицензию Creative Commons статьи, а ваше предполагаемое использование не разрешено законом или превышает разрешенное использование, вам необходимо получить разрешение непосредственно от правообладателя. Чтобы просмотреть копию этой лицензии, посетите http://creativecommons.org/licenses/by/4. 0/.
0/.
Перепечатки и разрешения
Об этой статье
Дополнительный белок Vpr ВИЧ-1 взаимодействует с REAF и ослабляет связанную с ним противовирусную активность
Новые результаты
Джозеф М. Гиббонс, Посмотреть профиль ORCIDКелли М. Марно, Ребекка Пайк, Посмотреть профиль ORCIDWing-yiu Джейсон Ли, Кристофер Э. Джонс, Б. В. Огунколейд, Клэр Пардье, Гэри Уорнс, Посмотреть профиль ORCIDПол Роули, Ричард Д. Слоан, Посмотреть профиль ORCIDÁine McKnight
doi: https://doi.org/10.1101/408161
- Abstract
- Full Text
- Info/History
- Metrics
- Preview PDF
Abstract
The accessory protein Vpr of Human Immunodeficiency Virus тип 1 (ВИЧ-1) усиливает репликацию вируса в макрофагах (1-7). Упакованный вирусной частицей Vpr высвобождается в клетках-мишенях вскоре после проникновения, что позволяет предположить, что он необходим на ранней стадии инфекции (8, 9). Почему он необходим для инфицирования макрофагов, а не циклических Т-клеток, и почему он вызывает остановку G2/M в циклических клетках, неизвестно. Здесь мы наблюдаем с помощью анализа ко-иммунопреципитации взаимодействие между Vpr и эндогенным REAF (РНК-ассоциированный противовирусный фактор ранней стадии, RPRD2), белком, который, как было показано ранее, сильно ограничивает ВИЧ-инфекцию (10). После того, как ВИЧ-1 инфицирует макрофаги, в течение 30 минут после проникновения вируса Vpr вызывает деградацию REAF. Впоследствии, по мере продолжения репликации, экспрессия REAF активируется — ответ, который ограничивается Vpr. REAF более выражен в дифференцированных макрофагах, чем в циклирующих Т-клетках. Экспрессия в циклических клетках зависит от клеточного цикла, и нокдаун вызывает нарушение клеточного цикла. Таким образом, наши результаты подтверждают давнюю гипотезу о том, что Vpr индуцирует деградацию фактора, участвующего в клеточном цикле, который препятствует ВИЧ-инфекции в макрофагах.
Почему он необходим для инфицирования макрофагов, а не циклических Т-клеток, и почему он вызывает остановку G2/M в циклических клетках, неизвестно. Здесь мы наблюдаем с помощью анализа ко-иммунопреципитации взаимодействие между Vpr и эндогенным REAF (РНК-ассоциированный противовирусный фактор ранней стадии, RPRD2), белком, который, как было показано ранее, сильно ограничивает ВИЧ-инфекцию (10). После того, как ВИЧ-1 инфицирует макрофаги, в течение 30 минут после проникновения вируса Vpr вызывает деградацию REAF. Впоследствии, по мере продолжения репликации, экспрессия REAF активируется — ответ, который ограничивается Vpr. REAF более выражен в дифференцированных макрофагах, чем в циклирующих Т-клетках. Экспрессия в циклических клетках зависит от клеточного цикла, и нокдаун вызывает нарушение клеточного цикла. Таким образом, наши результаты подтверждают давнюю гипотезу о том, что Vpr индуцирует деградацию фактора, участвующего в клеточном цикле, который препятствует ВИЧ-инфекции в макрофагах.
Резюме Вирус иммунодефицита человека типа 1 (ВИЧ-1) имеет так называемые вспомогательные белки, которые модулируют активность белков-хозяев, обеспечивая эффективную репликацию вируса. Точная функция одного из таких вспомогательных белков, Vpr, до сих пор не установлена. REAF представляет собой белок-хозяин, который ограничивает способность ВИЧ-1 инфицировать клетки. Здесь мы показываем, что Vpr взаимодействует с REAF. Вскоре после инфицирования, только при наличии Vpr, REAF разрушается в первичных макрофагах. Vpr дополнительно ограничивает последующее увеличение продукции REAF клетками. Кроме того, когда способность клетки продуцировать REAF предотвращается, популяция накапливается в фазе G2/M клеточного цикла. При инфекции Vpr отправляет клетки в стадию ареста G2/M. Таким образом, это исследование подтверждает давнюю гипотезу о том, что Vpr отвечает за деградацию клеточного фактора, участвующего в клеточном цикле и препятствующего завершению репликации ВИЧ-1.
Введение
Вирус иммунодефицита человека типа 1 (ВИЧ-1) инфицирует CD4 + Т-клетки и макрофаги in vivo и вызывает синдром приобретенного иммунодефицита (СПИД). ВИЧ-1 имеет четыре неструктурных дополнительных гена nef , vif , vpu и vpr , которые ослабляют врожденный иммунитет хозяина. Функция Vpr неясна, но она необходима для репликации в макрофагах и для патогенеза in vivo (1, 2). Значительные количества включаются в вирусные частицы и высвобождаются из основного капсидного белка (КА) после проникновения в клетку (8, 9).). Одновременно обратная транскрипция транскрибирует геном РНК в ДНК, которая интегрируется в ДНК клетки-хозяина. Он рано выпускается из CA (11), что позволяет предположить, что он имеет раннюю функцию вплоть до интеграции. Здесь мы показываем, что в течение 30 минут после проникновения в клетку вирус, содержащий Vpr, индуцирует деградацию РНК-ассоциированного противовирусного фактора ранней стадии (REAF, также известного как RPRD2). REAF, ранее описанный как Lv2, ограничивает завершение синтеза и интеграции провирусной ДНК (10).
REAF, ранее описанный как Lv2, ограничивает завершение синтеза и интеграции провирусной ДНК (10).
Результаты и обсуждение
HeLa-CD4, нокдаун по REAF (HeLa-CD4 shRNA-REAF, рис. 1A), 10 , были заражены ВИЧ-1 89,6 WT или вирус делетирован на vpr (89,6 Δ 9 vpr ), vif (89,6 Δ vif ) или vpu (89,6 Δ vpu ). На рис. 1В показано, что, несмотря на стандартное введение вируса (50 БОЕ/мл, как измерено на HeLa-CD4), удаление REAF с помощью кшРНК снижает потребность в Vpr. Существует значительно большее спасение от ВИЧ-1 89.6 Δ vpr (>60 раз, p <0,0001) по сравнению с HIV-1 89,6 WT или вирусом, лишенным vpu или vif (20 раз). Таким образом vpr преодолевает ограничение REAF.
Рисунок 1: Vpr ВИЧ-1 взаимодействует с REAF и преодолевает ограничения.
(A) Белок REAF в исходной HeLa-CD4 и HeLa-CD4, экспрессирующей кшРНК, нацеленную на REAF (HeLa-CD4 кшРНК-REAF). GAPDH — это контроль загрузки. (B) HeLa-CD4 shRNA-REAF, зараженный ВИЧ-1 89.6 WT или мутанты ВИЧ-1 89,6 Δ vpr , Δ vif или Δ vpu . HIV-1 89,6 Δ vpr более чем в 60 раз более чувствителен к рестрикции REAF, чем HIV-1 89,6 WT или другие мутанты. Ввод примерно 50 БОЕ/мл на HeLa-CD4. Столбики погрешностей указывают на стандартное отклонение, а звездочка указывает на статистическую значимость (****= p <0,0001, критерий Стьюдента). (C-E) Проточная цитометрия с визуализацией измеряла среднюю интенсивность флуоресценции (MFI) REAF в ядре (C) и цитоплазме (D) Hela-CD4 с течением времени после заражения ВИЧ-1 89.6 WT или ВИЧ-1 89,6 Δ впр . Результаты являются репрезентативными для трех отдельных экспериментов. Более низкий показатель обогащения ядра (E) указывает на то, что меньшая доля общего REAF находится в ядре ( p <0,05). Статистическую значимость рассчитывали по критерию Стьюдента. (F) Ко-иммунопреципитированный REAF был обнаружен с помощью вестерн-блоттинга VPR-GFP IP (справа), но не контрольного IP GFP (слева). (G) Вестерн-блоттинг REAF и HLTF в THP-1 с течением времени после заражения ВИЧ-1 89.6 ВТ . GAPDH — это контроль загрузки. (H) Вестерн-блоттинг MUS81 в Hela-CD4 с течением времени после заражения ВИЧ-1 89,1 WT . GAPDH — это контроль загрузки.
Более низкий показатель обогащения ядра (E) указывает на то, что меньшая доля общего REAF находится в ядре ( p <0,05). Статистическую значимость рассчитывали по критерию Стьюдента. (F) Ко-иммунопреципитированный REAF был обнаружен с помощью вестерн-блоттинга VPR-GFP IP (справа), но не контрольного IP GFP (слева). (G) Вестерн-блоттинг REAF и HLTF в THP-1 с течением времени после заражения ВИЧ-1 89.6 ВТ . GAPDH — это контроль загрузки. (H) Вестерн-блоттинг MUS81 в Hela-CD4 с течением времени после заражения ВИЧ-1 89,1 WT . GAPDH — это контроль загрузки.
REAF временно подавляется в HeLa-CD4 вскоре после инфицирования ВИЧ-1 (12). Здесь HeLa-CD4, инфицированные ВИЧ-1 89,6 WT или ВИЧ-1 89,6 Δ vpr , количественно определяли ядерный или цитоплазматический белок REAF с течением времени с помощью визуализации проточной цитометрии. После заражения ВИЧ-1 89.6 Δ vpr , уровни REAF увеличиваются как в ядре (~25%, рис. 1C), так и в цитоплазме (~10%, рис. 1D) в течение 30 минут, при этом ядерные уровни остаются высокими в течение 180 минут. Однако в присутствии Vpr (ВИЧ-1 89,6 WT ) это увеличение REAF прекращается через 30 минут с устойчивым снижением с течением времени. Снижение наиболее заметно в ядре со снижением примерно на 20% через 60 минут и примерно на 30% через 120 минут. К 180 минутам уровни REAF восстанавливаются.
1C), так и в цитоплазме (~10%, рис. 1D) в течение 30 минут, при этом ядерные уровни остаются высокими в течение 180 минут. Однако в присутствии Vpr (ВИЧ-1 89,6 WT ) это увеличение REAF прекращается через 30 минут с устойчивым снижением с течением времени. Снижение наиболее заметно в ядре со снижением примерно на 20% через 60 минут и примерно на 30% через 120 минут. К 180 минутам уровни REAF восстанавливаются.
Программное обеспечение для проточной цитометрии с визуализацией определяло «показатель обогащения ядер» с течением времени после инфицирования ВИЧ-1 89.6 WT или HIV-1 89,6 Δ vpr (рис. 1E). Чем ниже балл, тем меньше REAF в ядре по отношению к клетке в целом. К 60-120 минутам появляется значительное ( p <0,05) расслоение. В присутствии Vpr относительные ядерные уровни REAF подавляются между 30 и 120 минутами ( p <0,05). Более низкие уровни REAF также наблюдались в цитоплазме с течением времени, но в гораздо меньшей степени. Вирус несет ограниченное количество Vpr (11), что потенциально объясняет, почему уровни REAF возвращаются к норме или превышают ее к 180 минутам. Наши результаты подтверждают текущую модель активности Vpr — он взаимодействует с убиквитинлигазой E3 cullin4A-DDB1 (DCAF1) и индуцирует протеасомную деградацию неизвестного субстрата (13). Мы сообщили, что REAF расщепляется протеасомой при инфицировании ВИЧ-1 в HeLa-CD4 (12), что согласуется с этими наблюдениями. Кроме того, на рисунке 1F показано, что Vpr и REAF взаимодействуют друг с другом либо непосредственно, либо как часть комплекса, поскольку они совместно иммунопреципитируются. Это подтверждает наше предположение, что Vpr вызывает деградацию REAF.
Вирус несет ограниченное количество Vpr (11), что потенциально объясняет, почему уровни REAF возвращаются к норме или превышают ее к 180 минутам. Наши результаты подтверждают текущую модель активности Vpr — он взаимодействует с убиквитинлигазой E3 cullin4A-DDB1 (DCAF1) и индуцирует протеасомную деградацию неизвестного субстрата (13). Мы сообщили, что REAF расщепляется протеасомой при инфицировании ВИЧ-1 в HeLa-CD4 (12), что согласуется с этими наблюдениями. Кроме того, на рисунке 1F показано, что Vpr и REAF взаимодействуют друг с другом либо непосредственно, либо как часть комплекса, поскольку они совместно иммунопреципитируются. Это подтверждает наше предположение, что Vpr вызывает деградацию REAF.
Были предложены другие цели Vpr. Он привлекает эндонуклеазы SLX4-SLX1/MUS81-EME1 к DCAF1, активируя деградацию MUS81 и вызывая арест в G2/M (14). Он также разрушает геликазоподобный фактор транскрипции (HLTF) (15). Здесь мы показываем, что и HLTF (рис. 1G), и MUS81 (рис. 1H) истощаются вирусом одновременно с REAF в течение 60 минут после заражения. Интересно, что HLTF и REAF были идентифицированы в одном и том же скрининге белков, которые взаимодействуют с одноцепочечной ДНК (16). Ранее мы SS показали, что REAF связывает клеточную и вирусную ДНК и вирусные ДНК-содержащие обратные транскрипты (12). Истощение REAF после заражения носит временный характер, при этом восстановление через 120 минут, вероятно, отражает ограниченное количество Vpr, содержащегося в вирусной частице (11). Напротив, уровни HLTF и MUS81 остаются сниженными в течение по крайней мере 48 часов, что позволяет предположить, что они играют более позднюю роль в жизненном цикле вируса (9).1639 27 , 22 ). В отличие от REAF, ни SLX4-MUS81-EME1, ни HLTF до сих пор не были напрямую связаны с рестрикцией ВИЧ-1 (17).
Интересно, что HLTF и REAF были идентифицированы в одном и том же скрининге белков, которые взаимодействуют с одноцепочечной ДНК (16). Ранее мы SS показали, что REAF связывает клеточную и вирусную ДНК и вирусные ДНК-содержащие обратные транскрипты (12). Истощение REAF после заражения носит временный характер, при этом восстановление через 120 минут, вероятно, отражает ограниченное количество Vpr, содержащегося в вирусной частице (11). Напротив, уровни HLTF и MUS81 остаются сниженными в течение по крайней мере 48 часов, что позволяет предположить, что они играют более позднюю роль в жизненном цикле вируса (9).1639 27 , 22 ). В отличие от REAF, ни SLX4-MUS81-EME1, ни HLTF до сих пор не были напрямую связаны с рестрикцией ВИЧ-1 (17).
Мы определили фазу клеточного цикла (G1/0, S и G2/M) первичных моноцитов человека и проанализировали экспрессию REAF. Уровни самые низкие в G1, увеличиваются в фазе S и достигают максимума в G2/M (рис. 2А). Уровни REAF во время клеточного цикла дополнительно отслеживались после синхронизации на границе G2/M (рис. 2B, рис. S1). Когда синхронизированные клетки переключались с G2 на M, уровни REAF снижались, но восстанавливались через 8 часов. Основное снижение экспрессии REAF совпадает с фосфорилированием гистона h4 (Ser10/Thr11), митотического клеточного маркера (рис. 2В) (18).
2B, рис. S1). Когда синхронизированные клетки переключались с G2 на M, уровни REAF снижались, но восстанавливались через 8 часов. Основное снижение экспрессии REAF совпадает с фосфорилированием гистона h4 (Ser10/Thr11), митотического клеточного маркера (рис. 2В) (18).
Рис. S1. Графики проточной цитометрии клеточного цикла, сопровождающие рисунок 2B.
HeLa-CD4, синхронизированные на границе G2/M путем обработки нокодазолом, высвобождались из состояния остановки клеточного цикла, и им давали возможность перейти в митоз. Клетки, собранные с течением времени после высвобождения и окрашенные DAPI, анализировали на фазу клеточного цикла с помощью проточной цитометрии.
Рисунок 2: Экспрессия REAF колеблется в течение клеточного цикла, а истощение приводит к накоплению клеток G2/M.
(A) Визуализация проточной цитометрии фазы клеточного цикла и экспрессии REAF в окрашенных DAPI первичных моноцитах. (B) Экспрессия REAF в HeLa-CD4 в зависимости от времени после освобождения от остановки клеточного цикла, индуцированной нокодазолом. Фосфогистон h4 (Ser10/Thr11) представляет собой митотический маркер, а GAPDH представляет собой контроль загрузки. Были определены профили клеточного цикла, и соответствующие графики представлены на рисунке S1. (C-D) Визуализирующая проточная цитометрия субклеточных REAF в обработанном нокодазолом HeLa-CD4. Более низкий показатель обогащения ядер указывает на более низкую долю общего REAF в ядре — необработанные: 0,92, обработанные нокодазолом: 0,13 (одна популяция), 1,53 (другая популяция) (слева). Окрашивание фосфогистоном h4 (Ser28) подтвердило, что митотические клетки имели более низкий балл 0,17 (справа). Репрезентативные изображения (D) субклеточных REAF в митотических и немитотических клетках. (E) Конфокальная микроскопия субклеточных REAF в HeLa-CD4. Окрашивание фосфогистоном h4 (Ser28) и морфологию хроматина (Hoechst) использовали для идентификации фазы клеточного цикла.
(B) Экспрессия REAF в HeLa-CD4 в зависимости от времени после освобождения от остановки клеточного цикла, индуцированной нокодазолом. Фосфогистон h4 (Ser10/Thr11) представляет собой митотический маркер, а GAPDH представляет собой контроль загрузки. Были определены профили клеточного цикла, и соответствующие графики представлены на рисунке S1. (C-D) Визуализирующая проточная цитометрия субклеточных REAF в обработанном нокодазолом HeLa-CD4. Более низкий показатель обогащения ядер указывает на более низкую долю общего REAF в ядре — необработанные: 0,92, обработанные нокодазолом: 0,13 (одна популяция), 1,53 (другая популяция) (слева). Окрашивание фосфогистоном h4 (Ser28) подтвердило, что митотические клетки имели более низкий балл 0,17 (справа). Репрезентативные изображения (D) субклеточных REAF в митотических и немитотических клетках. (E) Конфокальная микроскопия субклеточных REAF в HeLa-CD4. Окрашивание фосфогистоном h4 (Ser28) и морфологию хроматина (Hoechst) использовали для идентификации фазы клеточного цикла. (F) Проточная цитометрия фазы клеточного цикла в окрашенных PI HeLa-CD4 shRNA-REAF (черный контур) и HeLa-CD4 (серый контур).
(F) Проточная цитометрия фазы клеточного цикла в окрашенных PI HeLa-CD4 shRNA-REAF (черный контур) и HeLa-CD4 (серый контур).
Используя визуализирующую проточную цитометрию, мы дополнительно проанализировали субклеточную локализацию REAF во время митоза (рис. 2C). Асинхронная популяция имела показатель ядерного обогащения 0,9.2. Клетки, обработанные нокодазолом, разделились на две популяции: одна с низким баллом (0,13), а другая с высоким баллом (1,53) (рис. 2С, слева). Фосфогистон h4 (Ser28), подтвержденный окрашиванием клеток в митозе, имел низкий балл 0,17 и, следовательно, более низкие уровни REAF в ядре по сравнению с клеткой в целом (рис. 2C, справа и 2D). Используя конфокальную микроскопию, REAF наблюдается как в цитоплазме, так и в ядре через интерфазу, профазу и прометафазу, но исключается из хроматина во время метафазы, анафазы и телофазы (рис. 2E). Кроме того, понижающая модуляция REAF в HeLa-CD4 shRNA-REAF вызывает накопление клеток в G2/M (рис. 2F). Проточная цитометрия содержания ДНК в клетках, окрашенных PI, показывает, что они накапливаются (25%) в G2/M по сравнению с исходными (14%).
2F). Проточная цитометрия содержания ДНК в клетках, окрашенных PI, показывает, что они накапливаются (25%) в G2/M по сравнению с исходными (14%).
Было показано, что Vpr в различной степени более полезен для репликации в макрофагах, чем в циклических Т-клетках (3-7) . Мы сравнили восприимчивость митотического HeLa-CD4 (92,5%) к асинхронной популяции (митотический 2,6%, рис. 3A) с использованием ВИЧ-1 89,6 (VSV-G) с репортером GFP в качестве контрольного вируса. Митотические клетки были в 12 раз более восприимчивы (рис. 3В). Это было подтверждено с использованием ВИЧ-1 89,6 WT , экспрессирующих оболочку ВИЧ-1 (рис. S2). Таким образом, исключение REAF из хроматина во время митоза может дать возможность избежать рестрикции в циклических Т-клетках. Результаты согласуются с предыдущими сообщениями о том, что остановка клеточного цикла в G2/M способствует ранней инфекции ВИЧ-1 (19).) и что существует отсроченная кинетика репликации мутантов vpr в Т-клетках (20). Рисунок 1 C-D выше предполагает, что ядерная интенсивность REAF является ключом к ограничению ВИЧ. Мы измерили экспрессию REAF в ядрах покоящихся или активированных CD4 + Т-клеток, моноцитах или макрофагах и дендритных клетках (ДК) (рис. 3С). Уровни экспрессии выше в MDM по сравнению с Т-клетками, что опять-таки совпадает с необходимостью Vpr ВИЧ-1 для заражения макрофагов, но не Т-клеток. Дифференциальная экспрессия белка REAF в моноцитах и MDM была подтверждена вестерн-блоттингом (рис. 3D).
Рисунок 1 C-D выше предполагает, что ядерная интенсивность REAF является ключом к ограничению ВИЧ. Мы измерили экспрессию REAF в ядрах покоящихся или активированных CD4 + Т-клеток, моноцитах или макрофагах и дендритных клетках (ДК) (рис. 3С). Уровни экспрессии выше в MDM по сравнению с Т-клетками, что опять-таки совпадает с необходимостью Vpr ВИЧ-1 для заражения макрофагов, но не Т-клеток. Дифференциальная экспрессия белка REAF в моноцитах и MDM была подтверждена вестерн-блоттингом (рис. 3D).
Рис. S2. Повышенная восприимчивость митотических клеток к ВИЧ-1.
HeLa-CD4, синхронизированные на границе G2/M обработкой тимидином/нокодазолом, были освобождены от остановки клеточного цикла и им позволили синхронно перейти в митоз на 2 часа, после чего их заразили ВИЧ-1 89,6 WT . Одновременно инфицировались асинхронные, необработанные HeLa-CD4. Вирусную инфекционность оценивали через 48 часов после заражения путем внутриклеточного окрашивания р24 ВИЧ-1 для выявления фокусообразующих единиц (ФОЕ) (слева). Проточную цитометрию использовали для определения профилей клеточного цикла клеток во время инфекции с использованием окрашивания DAPI для определения содержания ДНК и антитела против фосфогистона h4 (Ser28) для идентификации митотических клеток (в центре). Вестерн-блоттинг использовали для подтверждения обогащенной популяции митотических клеток в синхронизированной популяции с использованием фосфогистона h4 (Ser10/Thr11) в качестве альтернативного маркера митотических клеток и GAPDH в качестве контроля нагрузки (справа).
Проточную цитометрию использовали для определения профилей клеточного цикла клеток во время инфекции с использованием окрашивания DAPI для определения содержания ДНК и антитела против фосфогистона h4 (Ser28) для идентификации митотических клеток (в центре). Вестерн-блоттинг использовали для подтверждения обогащенной популяции митотических клеток в синхронизированной популяции с использованием фосфогистона h4 (Ser10/Thr11) в качестве альтернативного маркера митотических клеток и GAPDH в качестве контроля нагрузки (справа).
Рисунок 3: Митотические клетки более восприимчивы к инфекции ВИЧ-1. Vpr подавляет REAF в MDM.
(A, B) HeLa-CD4, обработанный тимидином/нокодазолом, освобождался от остановки клеточного цикла на границе G2/M. Через 2 часа цикла митоза их и необработанный HeLa-CD4 трижды заражали ВИЧ-1 89,6 (VSV-G) с репортером GFP. Проточная цитометрия подтвердила, что синхронизированная популяция была значительно обогащена митотическими клетками во время заражения (идентифицировано с использованием фосфогистона h4 (Ser28)) (A). Кратность увеличения вирусной инфекционности оценивали через 48 часов после заражения с помощью проточной цитометрии. Флуоресценция GFP идентифицировала инфицированные клетки (B). (C) Ядерная экспрессия REAF в указанных типах клеток от двух доноров крови, измеренная с помощью проточной цитометрии. (D) Вестерн-блоттинг экспрессии REAF во время дифференцировки моноцитов в макрофаги с M-CSF. GAPDH — это контроль загрузки. (E) Белок REAF в обработанном поли(I:C), дифференцированном PMA, THP-1. GAPDH — это контроль загрузки. (F, G) MDM были заражены ВИЧ-1 89,6 WT (F) или ВИЧ-1 89,6 Δ vpr (G), собраны в указанное время после заражения и проанализированы на экспрессию REAF. GAPDH — это контроль загрузки. Представлен денситометрический количественный анализ 200 кДа REAF. (H, I) МДМ, зараженные ВИЧ-1 89,6 WT или ВИЧ-1 89,6 Δ vpr , анализировали методом проточной цитометрии на предмет экспрессии REAF в ядре (H) и цитоплазме (I) в указанное время после вызова.
Кратность увеличения вирусной инфекционности оценивали через 48 часов после заражения с помощью проточной цитометрии. Флуоресценция GFP идентифицировала инфицированные клетки (B). (C) Ядерная экспрессия REAF в указанных типах клеток от двух доноров крови, измеренная с помощью проточной цитометрии. (D) Вестерн-блоттинг экспрессии REAF во время дифференцировки моноцитов в макрофаги с M-CSF. GAPDH — это контроль загрузки. (E) Белок REAF в обработанном поли(I:C), дифференцированном PMA, THP-1. GAPDH — это контроль загрузки. (F, G) MDM были заражены ВИЧ-1 89,6 WT (F) или ВИЧ-1 89,6 Δ vpr (G), собраны в указанное время после заражения и проанализированы на экспрессию REAF. GAPDH — это контроль загрузки. Представлен денситометрический количественный анализ 200 кДа REAF. (H, I) МДМ, зараженные ВИЧ-1 89,6 WT или ВИЧ-1 89,6 Δ vpr , анализировали методом проточной цитометрии на предмет экспрессии REAF в ядре (H) и цитоплазме (I) в указанное время после вызова. (J) Заразность ВИЧ-1 89.6 WT по сравнению с ВИЧ-1 89,6 Δ vpr в первичных макрофагах человека. Вирусный ввод был эквивалентен 50 нг.
(J) Заразность ВИЧ-1 89.6 WT по сравнению с ВИЧ-1 89,6 Δ vpr в первичных макрофагах человека. Вирусный ввод был эквивалентен 50 нг.
Противовирусные факторы часто активируются в ответ на молекулярные паттерны, связанные с патогенами. Полирибоинозиновая:полирибоцитидиловая кислота (поли(I:C)) представляет собой двухцепочечную РНК, используемую для стимуляции путей распознавания молекулярных паттернов, связанных с вирусной инфекцией. На фигуре 3E показана поли(I:C) индукция REAF в THP-1, клеточной линии макрофагов.
Чтобы расшифровать роль Vpr и REAF в первичных макрофагах, МДМ заражали ВИЧ-1 89.6 WT или ВИЧ-1 89,6 Δ впр . Вестерн-блоттинг показывает, что уровни REAF снижаются в течение 30 и вплоть до 60 минут после заражения ВИЧ-1 89,6 WT (рис. 3F). Базальные уровни возвращаются к 240 минутам. Это контрастирует с инфекцией ВИЧ-1 89,6 Δ vpr , при которой уровни REAF не снижаются и даже повышаются с 60 до 240 минут (рис. 3G). Таким образом, MDM реагируют на инфекцию ВИЧ-1, активируя REAF, но Vpr смягчает это, вызывая деградацию REAF.
3G). Таким образом, MDM реагируют на инфекцию ВИЧ-1, активируя REAF, но Vpr смягчает это, вызывая деградацию REAF.
Субклеточные колебания уровней REAF у MDM после заражения ВИЧ-1 89,6 WT или ВИЧ-1 89,6 Δ vpr определяли с помощью проточной цитометрии с визуализацией. С Vpr ядерная REAF снижается между 60 и 120 минутами (P <0,05, рис. 3H), аналогично HeLa-CD4. Напротив, без vpr ядерная REAF увеличивается на 120-й минуте (примерно на 25%). Подобно ответу на поли(I:C) в THP-1, цитоплазматическая экспрессия REAF увеличивается в течение 30 минут после заражения любым вирусом (рис. 3I). Интересно, что цитоплазматическая активация REAF была даже выше для ВИЧ-1 89..6 WT , чем для мутантного вируса без Vpr, что, возможно, отражает исключение из ядра. Эти результаты подтверждают предположение, что Vpr преодолевает ограничение REAF при MDM, где экспрессия REAF высока и дополнительно индуцируется репликацией вируса. Фигура 3J подтверждает, что вирус ВИЧ-1 89,6 Δ vpr , использованный в этих экспериментах, ограничен репликацией в MDM по сравнению с вирусом дикого типа, экспрессирующим Vpr (ВИЧ-1 89,6 WT ).
REAF обладает многими свойствами рестрикционных факторов (21, 22). Он взаимодействует с обратными транскриптами ВИЧ-1, препятствуя обратной транскрипции и интеграции (12). Он кодируется зародышевой линией, конститутивно экспрессируется в клетках, регулируется протеасомной системой, подавляется Vpr и активируется поли(I:C).
IFNα индуцирует многие факторы рестрикции ВИЧ (23, 24). Мы использовали RNA-Seq, чтобы определить, активирует ли IFNα мРНК REAF при MDM. На рис. 4А показана активация противовирусных генов, индуцированная IFNα, включая факторы рестрикции ВИЧ APOBEC3G, IFITM1-3, MX2, тетерин и виперин (21), но с незначительной активацией мРНК REAF или без нее. Кроме того, не было изменений ни в субклеточном распределении, ни в общих уровнях с помощью вестерн-блоттинга или проточной цитометрии (у некоторых доноров наблюдалось небольшое увеличение с помощью вестерн-блоттинга, рисунок S3). Также не было экспрессии мРНК или белка REAF в CD4 9.0412 + Т-клеток (рис. S4) или в THP-1 в ответ на IFN α, β или γ (рис. S5).
S4) или в THP-1 в ответ на IFN α, β или γ (рис. S5).
Рис. S3. Никакой IFN не индуцировал увеличение экспрессии белка REAF или изменение субклеточного распределения при MDM.
(A) MDM трех доноров лечили IFNα (100 МЕ/мл) в течение 24 часов. Вестерн-блоттинг (слева) и визуализирующая проточная цитометрия (справа) использовались для определения уровня белка REAF и субклеточного распределения с лечением и без него. IFITM3 использовали в качестве положительного контроля для индуцированного IFN повышения уровня белка, а GAPDH — в качестве контроля нагрузки. (B) Визуализирующая проточная цитометрия экспрессии REAF (слева) и IFITM1 (справа) в MDM от другого донора, получавшего указанные IFN (100 МЕ/мл) в течение 24 часов. Экспрессия IFITM3 (справа) использовалась в качестве положительного контроля для активации белка.
Рисунок 4: REAF не стимулируется IFN или подвергается положительной селекции.
(A) RNA-Seq определил изменение мРНК REAF по сравнению с другими противовирусными факторами у MDM, получавших IFNα (500 МЕ/мл). (B) Последовательности ДНК REAF от 15 существующих видов приматов (длина дерева 0,2 замены на сайт по всем ветвям филогении) (вверху) были проанализированы с использованием пакета PAML на признаки положительного естественного отбора (внизу). Начальные начальные значения для ω (ω O ), и различные модели частоты кодонов использовались в моделировании максимального правдоподобия. Двойная разница натуральных логарифмов правдоподобия (2*◻ InL) двух моделей была рассчитана и оценена с использованием критического значения хи-квадрат. Значение р указывает, с какой уверенностью нулевая модель (М1, М7, М8а) может быть отвергнута в пользу модели положительного отбора (М2, М8).
Факторы рестрикции часто подвергаются эволюционному положительному отбору в местах, которые взаимодействуют с вирусом. Мы не нашли доказательств положительного отбора REAF в линии приматов (рис. 4B), и поэтому он лучше соответствует модели очищающего отбора. Это может отражать роль в развитии G2/M, исключая изменения его первичной последовательности. REAF отличается от эволюционирующих факторов рестрикции ВИЧ, таких как APOBEC3G, SAMHD1, TRIM5 или BST2/тетерин, и больше похож на SERINC3 и 5, которые не подвергаются положительной селекции (25, 26). Мы предполагаем, что REAF является многофункциональным или «подрабатывающим» белком, выполняющим как минимум две клеточные роли (27). В циклических Т-клетках REAF связан с переходом G2/M, поэтому его истощение с помощью Vpr вызывает накопление G2/M. В нециклирующих клетках Vpr важен для ВИЧ-инфекции макрофагов, где REAF высоко экспрессирован.
4B), и поэтому он лучше соответствует модели очищающего отбора. Это может отражать роль в развитии G2/M, исключая изменения его первичной последовательности. REAF отличается от эволюционирующих факторов рестрикции ВИЧ, таких как APOBEC3G, SAMHD1, TRIM5 или BST2/тетерин, и больше похож на SERINC3 и 5, которые не подвергаются положительной селекции (25, 26). Мы предполагаем, что REAF является многофункциональным или «подрабатывающим» белком, выполняющим как минимум две клеточные роли (27). В циклических Т-клетках REAF связан с переходом G2/M, поэтому его истощение с помощью Vpr вызывает накопление G2/M. В нециклирующих клетках Vpr важен для ВИЧ-инфекции макрофагов, где REAF высоко экспрессирован.
Материалы и методы
Заявление об этике
Конусы с лейкоцитами от доноров крови, из которых были выделены РВМС, были получены из службы переливания крови NHS, госпиталь Св. Георгия, Лондон. Доноры были анонимными, поэтому согласие пациента не требовалось. Местный идентификационный номер этического сертификата: 06/Q0603/59.
Клеточные линии
HEK-293T (ATCC), THP-1, C8166, исходный HeLa-CD4 (все реагенты NIBSC AIDS) и shRNA-REAF (HeLa-CD4 shRNA-REAF, описанный ранее) поддерживали при 37°С.0412° С в 5% СО 2 (10). Клетки выращивали в среде Игла, модифицированной Дульбекко (DMEM, ThermoFisher), с добавлением эмбриональной бычьей сыворотки (5-10%, Thermo Fisher) и соответствующих антибиотиков. HeLa-CD4-shRNA-REAF отбирали по устойчивости к пуромицину в среде с добавлением 10 мкг/мл пуромицина.
Трансфекции и продукция вируса
Инфекционный молекулярный клон ВИЧ-1 89.6 был получен из Центра исследований СПИДа (NIBSC, Великобритания). Инфекционные полноразмерные и химерные клоны ВИЧ получали путем трансфекции HEK-29 линейным полиэтиленимином 25К (Polysciences), липофектамином 2000 (Invitrogen) или липофектамином 3000 (Invitrogen).3т. Плазмидные конструкции HIV-1 89,6 Δ vif , HIV-1 89,6 Δ vpr и HIV-1 89,6 Δ vpu были созданы с использованием молекулярного клона HIV-1 9, перекрывающегося 3 ПЦР. (24) . Клоны были подтверждены секвенированием плазмид (Source BioScience). Последовательности праймеров доступны по запросу.
(24) . Клоны были подтверждены секвенированием плазмид (Source BioScience). Последовательности праймеров доступны по запросу.
HEK-293T высевали в количестве 2×10 4 /см 2 в 8-луночные предметные стекла (конфокальная микроскопия) или чашки 10 см (выработка вируса) за 48 часов до трансфекции. Для продукции вируса супернатант собирали через 72 часа после трансфекции и очищали от клеточного дебриса центрифугированием при 500×9.1639 г за 5 минут до хранения при -80 ° С. Мутантный вирус с низким титром амплифицировали с помощью С8166 за 48 часов до сбора. ВИЧ-1 89.6 (VSV-G) был создан путем объединения вектора переноса pCSGW с оболочкой pMDG VSV-G и центральной конструкцией p8.91-89.6 gag в HEK-293T, как указано выше, и был описан ранее (12). ) .
Титрование компетентного к репликации вируса
HeLa-CD4 высевали в количестве 1,5×10 4 клеток/лунку в 48-луночные планшеты с образованием прикрепленного монослоя клеток. Монослои клеток заражали серийными разведениями 1/5 вируса, и титр оценивали через 48 часов с помощью in situ внутриклеточное окрашивание р24 ВИЧ-1 для идентификации отдельных очагов репликации вируса (БОЕ), как описано ранее (12) . Для экспериментов с течением времени заражения 400-500 мкл вируса 1×10 5 БОЕ/мл (HeLa-CD4) или 3×10 3 БОЕ/мл (MDM) добавляли на лунку к клеткам, культивируемым в 6-луночных планшетах. на 24 часа (HeLa-CD4) или 7 дней (для МДМ). На фигуре 3J клетки заражали 50 нг p24 в 6-луночных планшетах с 2×10 6 MDM на лунку. Супернатанты собирали на 0, 2, 8, 21 и 28 дни после контрольного заражения и анализировали концентрацию p24 с помощью ELISA.
Монослои клеток заражали серийными разведениями 1/5 вируса, и титр оценивали через 48 часов с помощью in situ внутриклеточное окрашивание р24 ВИЧ-1 для идентификации отдельных очагов репликации вируса (БОЕ), как описано ранее (12) . Для экспериментов с течением времени заражения 400-500 мкл вируса 1×10 5 БОЕ/мл (HeLa-CD4) или 3×10 3 БОЕ/мл (MDM) добавляли на лунку к клеткам, культивируемым в 6-луночных планшетах. на 24 часа (HeLa-CD4) или 7 дней (для МДМ). На фигуре 3J клетки заражали 50 нг p24 в 6-луночных планшетах с 2×10 6 MDM на лунку. Супернатанты собирали на 0, 2, 8, 21 и 28 дни после контрольного заражения и анализировали концентрацию p24 с помощью ELISA.
Синтез кДНК и количественная ПЦР
Тотальную РНК экстрагировали из MDM с помощью набора RNeasy Plant Mini Kit (QIAGEN), а кДНК синтезировали с помощью системы синтеза первой нити SuperScript™ III (Invitrogen) в соответствии с инструкциями производителя. кДНК подвергали количественной ПЦР в реальном времени (кПЦР) с использованием пар праймеров REAF, OAS1 и β-актина с детектированием амплифицированных транскриптов SYBR ® Green (набор QuantiTect SYBR Green PCR Kit, QIAGEN). Сбор и анализ данных проводили с использованием программного обеспечения ABI PRISM™ 7500 SDS. Последовательности праймеров доступны по запросу.
кДНК подвергали количественной ПЦР в реальном времени (кПЦР) с использованием пар праймеров REAF, OAS1 и β-актина с детектированием амплифицированных транскриптов SYBR ® Green (набор QuantiTect SYBR Green PCR Kit, QIAGEN). Сбор и анализ данных проводили с использованием программного обеспечения ABI PRISM™ 7500 SDS. Последовательности праймеров доступны по запросу.
Микрочип экспрессии генов
Перед анализом микрочипов РНК MDM готовили с использованием набора для амплификации РНК Illumina™ TotalPrep™ (Ambion) в соответствии с инструкциями производителя. Зонды гибридизовали на массиве шариков Illumina™ HT12v3 в соответствии со стандартными протоколами гибридизации и сканирования производителя. Необработанные измерения были обработаны с помощью программного обеспечения GenomeStudio (Illumina) и нормализованы по квантилям. Все данные микрочипов общедоступны в базе данных Gene Expression Omnibus (GEO) с регистрационным номером GSE54455.
IFN, Poly(I:C) и обработка
MDM, CD4 + Т-клетки и THP-1 обрабатывали IFN (100-500 МЕ/мл, указано) в течение 24 или 48 часов (уточнено) перед сбором для выделения РНК; анализ с помощью вестерн-блоттинга или проточной цитометрии. THP-1 обрабатывали поли(I:C) (25 мкг/мл, HMW/LyoVec™, Invitrogen) в течение 48 часов перед анализом с помощью вестерн-блоттинга или проточной цитометрии с визуализацией. Перед обработкой IFN или поли(I:C) THP-1 обрабатывали форбол-12-миристат-13-ацетатом (PMA, 62 нг/мл) в течение 3 дней, а затем DMEM без PMA в течение 2 дней, чтобы обеспечить дифференцировку и восстановление . Для рис. 4B и рис. S4 рекомбинантный IFNα был приобретен у Sigma (человеческий интерферон-α/D, каталожный номер I4401-100KU) и представляет собой комбинацию человеческих подтипов 1 и 2. Для рис. Пепротех.
THP-1 обрабатывали поли(I:C) (25 мкг/мл, HMW/LyoVec™, Invitrogen) в течение 48 часов перед анализом с помощью вестерн-блоттинга или проточной цитометрии с визуализацией. Перед обработкой IFN или поли(I:C) THP-1 обрабатывали форбол-12-миристат-13-ацетатом (PMA, 62 нг/мл) в течение 3 дней, а затем DMEM без PMA в течение 2 дней, чтобы обеспечить дифференцировку и восстановление . Для рис. 4B и рис. S4 рекомбинантный IFNα был приобретен у Sigma (человеческий интерферон-α/D, каталожный номер I4401-100KU) и представляет собой комбинацию человеческих подтипов 1 и 2. Для рис. Пепротех.
Рис. S4. IFN не индуцировал активацию мРНК REAF в MDM или CD4+ T-клетках и не вызывал активацию белка в CD4+ T-клетках.
MDM и первичные CD4 + Т-клетки обрабатывали IFNα (500 МЕ/мл) в течение 48 часов. Увеличение мРНК REAF по сравнению с β-актином измеряли с помощью количественной ПЦР, а OAS1 использовали в качестве положительного контроля для индуцированной IFN повышающей регуляции (слева). Экспрессию белка REAF (справа) также измеряли в Т-клетках CD4 + с помощью вестерн-блоттинга с GAPDH в качестве контроля нагрузки.
Экспрессию белка REAF (справа) также измеряли в Т-клетках CD4 + с помощью вестерн-блоттинга с GAPDH в качестве контроля нагрузки.
Рис. S5. Отсутствует активация экспрессии белка REAF в обработанном IFN PMA, дифференцированном THP-1.
PMA-дифференцированный THP-1 анализировали вестерн-блоттингом после обработки указанными интерферонами (100 МЕ/мл) в течение 24 часов. Указаны полосы 200 и 80 кДа, не все полосы REAF обнаруживаются во всех экспериментах. IFITM1 использовали в качестве положительного контроля для индуцированного IFN повышения уровня белка, а β-актин использовали в качестве контроля нагрузки.
Вестерн-блоттинг
Клетки собирали и лизировали в 30-50 мкл буфера для радиоиммунопреципитации (RIPA) с добавлением NaF (5 мкМ), Na 2 VO 3 (5 мкМ), β-глицерофосфат (5 мкМ) и 1 коктейль ингибиторов протеазы (цитоскелет). Концентрацию белка в каждом образце определяли с использованием набора для анализа белка BCA (Pierce). 25 мкг или 12,5 мкг общего белка разделяли с помощью SDS-PAGE (4-12% Bis-Tris Gel, Invitrogen) при 130 В в течение 1 часа 30 минут в прогонном буфере MOPS SDS (Invitrogen). Разделенные белки переносили на нитроцеллюлозную мембрану (размер пор 0,45 мкм, GE Healthcare) при 45 В в течение 2 часов в охлажденном льдом буфере для переноса NuPAGE™ (ThermoFisher). Мембраны блокировали в течение 1 часа при комнатной температуре в 5% (мас./об.) обезжиренного сухого молока в буфере TBST. Специфические белки выявляли первичными антителами путем инкубации с мембранами в течение ночи при 4 ° С и со вторичными антителами в течение 1 часа при комнатной температуре. Все антитела разводили блокирующим буфером. Белки визуализировали с использованием реагента для детекции вестерн-блоттинга ECL Prime (GE Healthcare) и визуализировали либо с помощью системы визуализации гелей ChemiDoc (Bio-Rad), либо экспонировали с пленками CL-XPosure (ThermoScientific) и проявляли.
25 мкг или 12,5 мкг общего белка разделяли с помощью SDS-PAGE (4-12% Bis-Tris Gel, Invitrogen) при 130 В в течение 1 часа 30 минут в прогонном буфере MOPS SDS (Invitrogen). Разделенные белки переносили на нитроцеллюлозную мембрану (размер пор 0,45 мкм, GE Healthcare) при 45 В в течение 2 часов в охлажденном льдом буфере для переноса NuPAGE™ (ThermoFisher). Мембраны блокировали в течение 1 часа при комнатной температуре в 5% (мас./об.) обезжиренного сухого молока в буфере TBST. Специфические белки выявляли первичными антителами путем инкубации с мембранами в течение ночи при 4 ° С и со вторичными антителами в течение 1 часа при комнатной температуре. Все антитела разводили блокирующим буфером. Белки визуализировали с использованием реагента для детекции вестерн-блоттинга ECL Prime (GE Healthcare) и визуализировали либо с помощью системы визуализации гелей ChemiDoc (Bio-Rad), либо экспонировали с пленками CL-XPosure (ThermoScientific) и проявляли.
Антитела
Ранее было описано первичное кроличье поликлональное антитело к REAF (RbpAb-RPRD2) (12). Для визуализирующей проточной цитометрии и конфокальной микроскопии RbpAb-RPRD2 выявляли с использованием козьего антикроличьего IgG, конъюгированного с Alexa Fluor 647 (Invitrogen). Меченый FITC антифосфогистон h4 (Ser28) использовали (BD Bioscience) для визуализации проточной цитометрии и конфокальной микроскопии. MsmAb-IFITM1 (клон 5B5E2, Proteintech) выявляли с помощью козьего антимышиного IgG Alexa Fluor 555 (ThermoFisher) для визуализации проточной цитометрии и с помощью антимышиного IgG-антитела, конъюгированного с HRP (GE Healthcare) для Вестерн-блоттинга, как и MsmAb. -Mus81 и MsmAb-GFP (оба Abcam). Также для Вестерн-блоттинга RbpAb-RPRD2, RbmAb-IFITM3 (EPR5242, Insight Biotechnology), RbpAb-GAPDH, RbpAb-βActin, RbmAb-фосфогистон h4 (Ser10/Thr11) и RbpAb-HLTF (все Abcam) были обнаружены с помощью вторичного антитело: ослиный антикроличий IgG, конъюгированный с HRP (GE Healthcare).
Для визуализирующей проточной цитометрии и конфокальной микроскопии RbpAb-RPRD2 выявляли с использованием козьего антикроличьего IgG, конъюгированного с Alexa Fluor 647 (Invitrogen). Меченый FITC антифосфогистон h4 (Ser28) использовали (BD Bioscience) для визуализации проточной цитометрии и конфокальной микроскопии. MsmAb-IFITM1 (клон 5B5E2, Proteintech) выявляли с помощью козьего антимышиного IgG Alexa Fluor 555 (ThermoFisher) для визуализации проточной цитометрии и с помощью антимышиного IgG-антитела, конъюгированного с HRP (GE Healthcare) для Вестерн-блоттинга, как и MsmAb. -Mus81 и MsmAb-GFP (оба Abcam). Также для Вестерн-блоттинга RbpAb-RPRD2, RbmAb-IFITM3 (EPR5242, Insight Biotechnology), RbpAb-GAPDH, RbpAb-βActin, RbmAb-фосфогистон h4 (Ser10/Thr11) и RbpAb-HLTF (все Abcam) были обнаружены с помощью вторичного антитело: ослиный антикроличий IgG, конъюгированный с HRP (GE Healthcare).
Иммунопреципитация. глицерофосфат (5 мкМ) и 1x коктейль ингибиторов протеаз (цитоскелет).
 Концентрацию общего белка определяли с использованием набора для анализа белков BCA (Pierce). Магнитные агарозные шарики GFP-TRAP ® уравновешивали в охлажденном льдом буфере для разбавления (10 мМ Трис/Cl, рН 7,5; 150 мМ NaCl; 0,5 мМ ЭДТА) в соответствии с инструкциями производителя (Chromotek). Клеточные лизаты, содержащие 100 мкг общего белка, инкубировали с 10 мкл уравновешенных гранул в течение 2 часов при 4–9°С.0412° С при осторожном встряхивании. Гранулы трижды промывали буфером PBST перед анализом вестерн-блоттингом.
Концентрацию общего белка определяли с использованием набора для анализа белков BCA (Pierce). Магнитные агарозные шарики GFP-TRAP ® уравновешивали в охлажденном льдом буфере для разбавления (10 мМ Трис/Cl, рН 7,5; 150 мМ NaCl; 0,5 мМ ЭДТА) в соответствии с инструкциями производителя (Chromotek). Клеточные лизаты, содержащие 100 мкг общего белка, инкубировали с 10 мкл уравновешенных гранул в течение 2 часов при 4–9°С.0412° С при осторожном встряхивании. Гранулы трижды промывали буфером PBST перед анализом вестерн-блоттингом.
Магнитное разделение первичных лимфоцитов человека
Мононуклеарные клетки периферической крови (МКПК) выделяли из лейкоцитарных конусов (служба переливания крови NHS, больница Св. Георгия, Лондон) путем центрифугирования в градиенте плотности со средой в градиенте плотности Lymphoprep™ (STEMCELL™ Technologies) . Периферические моноциты выделяли из РВМС с использованием CD14 9 человека.0412 + магнитные шарики (Miltenyi Biotech) согласно инструкции производителя. CD4 + Т-клетки выделяли из потока с использованием набора для выделения человеческих CD4 + Т-клеток (Miltenyi Biotech). CD14 + моноцитов и CD4 + Т-клетки либо дифференцировали, либо фиксировали сразу после выделения для внутриклеточного окрашивания. Для получения макрофагов M1 и M2 (M1/M2 MDM) моноциты обрабатывали либо гранулоцитарно-макрофагальным колониестимулирующим фактором (GM-CSF, 100 нг/мл, Peprotech), либо макрофагальным колониестимулирующим фактором (M-CSF, 100 нг/мл) для 7 дней, с пополнением среды на 4-й день. Для получения дендритных клеток (ДК) моноциты обрабатывали GM-CSF (50 нг/мл) и IL-4 (50 нг/мл) в течение 7 дней с пополнением среды на 4-й день. Активированный CD4 + Т-клетки были получены путем стимуляции свежевыделенных CD4 + Т-клеток в концентрации 1×10 6 /мл с активатором Т-клеток CD3/CD28 Dynabeads (ThermoFisher) при соотношении шариков к клеткам, равном 1, на 7 дней. Перед внутриклеточным окрашиванием и проточной цитометрией удаляли магнитные шарики.
CD4 + Т-клетки выделяли из потока с использованием набора для выделения человеческих CD4 + Т-клеток (Miltenyi Biotech). CD14 + моноцитов и CD4 + Т-клетки либо дифференцировали, либо фиксировали сразу после выделения для внутриклеточного окрашивания. Для получения макрофагов M1 и M2 (M1/M2 MDM) моноциты обрабатывали либо гранулоцитарно-макрофагальным колониестимулирующим фактором (GM-CSF, 100 нг/мл, Peprotech), либо макрофагальным колониестимулирующим фактором (M-CSF, 100 нг/мл) для 7 дней, с пополнением среды на 4-й день. Для получения дендритных клеток (ДК) моноциты обрабатывали GM-CSF (50 нг/мл) и IL-4 (50 нг/мл) в течение 7 дней с пополнением среды на 4-й день. Активированный CD4 + Т-клетки были получены путем стимуляции свежевыделенных CD4 + Т-клеток в концентрации 1×10 6 /мл с активатором Т-клеток CD3/CD28 Dynabeads (ThermoFisher) при соотношении шариков к клеткам, равном 1, на 7 дней. Перед внутриклеточным окрашиванием и проточной цитометрией удаляли магнитные шарики.
Иммунофлуоресценция
Трансфицированные клетки промывали PBS и фиксировали в 2% параформальдегиде/PBS в течение 10 минут при комнатной температуре. Затем фиксированные клетки пермеабилизировали в 0,2% Triton-X100/PBS в течение 20 минут при комнатной температуре. Клетки инкубировали с первичными антителами в PBS, содержащем 0,1 % Triton-X100 и 2 % BSA, в течение ночи при 4–°°С. После 3 промывок в PBS клетки затем метили вторичными антителами в том же буфере в течение 1 часа при комнатной температуре и 3 раза промывали PBS. Для конфокальной микроскопии ядра докрашивали Hoechst 33342 (2 мкМ, ThermoFisher) в течение 5 минут при комнатной температуре. Меченые клетки помещали в ProLong™ Diamond Antifade Mountant (ThermoFisher) и анализировали на лазерном сканирующем конфокальном микроскопе LSM 710 (Carl Zeiss). Изображения были получены с помощью программного обеспечения ZEN и проанализированы с помощью ImageJ.
Проточная цитометрия с визуализацией
Клетки фиксировали в FIX&PERM ® Solution A (Nordic MUbio) в течение 30 минут и пермеабилизировали 0,2% Triton™-X 100/PBS. МДМ блокировали сывороткой человека (1%). Используемый буфер для окрашивания представлял собой: 0,1% Triton™-X 100 0,5% FCS. Ядра окрашивали DAPI (1 мкг/мл) в течение двух часов. Визуализирующую проточную цитометрию выполняли с использованием проточного цитометра Amnis ImageStream ®x Mark II (Merck) и программного обеспечения INSPIRE ® (Amnis). Для каждого образца было собрано не менее 10 000 событий, стратегия гейтирования показана на рисунке S6. ИДЕИ 9Программное обеспечение 0412® (Amnis) использовалось для анализа и определения «оценки ядерного обогащения». Оценка обогащения ядра представляет собой сравнение интенсивности флуоресценции REAF внутри ядра с общей интенсивностью флуоресценции всей клетки. Более низкий показатель обогащения ядра указывает на то, что меньшая доля общего REAF находится внутри ядра.
МДМ блокировали сывороткой человека (1%). Используемый буфер для окрашивания представлял собой: 0,1% Triton™-X 100 0,5% FCS. Ядра окрашивали DAPI (1 мкг/мл) в течение двух часов. Визуализирующую проточную цитометрию выполняли с использованием проточного цитометра Amnis ImageStream ®x Mark II (Merck) и программного обеспечения INSPIRE ® (Amnis). Для каждого образца было собрано не менее 10 000 событий, стратегия гейтирования показана на рисунке S6. ИДЕИ 9Программное обеспечение 0412® (Amnis) использовалось для анализа и определения «оценки ядерного обогащения». Оценка обогащения ядра представляет собой сравнение интенсивности флуоресценции REAF внутри ядра с общей интенсивностью флуоресценции всей клетки. Более низкий показатель обогащения ядра указывает на то, что меньшая доля общего REAF находится внутри ядра.
Рис. S6. Стратегия последовательного стробирования, используемая в анализе проточной цитометрии изображений с помощью программного обеспечения IDEAS.
(А) Отдельные клетки были отобраны по соотношению площади и соотношения сторон светлопольных изображений клеток. (B) Клетки с изображениями в фокусе были отобраны по RMS градиента (среднеквадратичное значение скорости изменения профиля интенсивности изображения). Показаны репрезентативные примеры сюжетов.
Статистика
Статистическую значимость во всех экспериментах рассчитывали с помощью критерия Стьюдента (двусторонний). Данные представлены как среднее значение ± стандартное отклонение (планки погрешностей). Для расчета и иллюстрации графиков использовались GraphPad Prism и Excel.
Синхронизация клеток
HeLa-CD4 синхронизировали на границе G2/M нокодазолом (200 нг/мл) в течение 16 часов. Там, где синхронизированные клетки были инфицированы вирусом, индуцировали начальную S-фазу блокады тимидином (4 мМ) в течение 24 часов с последующей промывкой PBS и обработкой нокодазолом (100 нг/мл) в течение еще 16 часов. Сбор только тех клеток, которые находились в суспензии, а также тех, которые легко отделялись при ручном «стряхивании», обогащал популяцию митотических клеток.
Сбор только тех клеток, которые находились в суспензии, а также тех, которые легко отделялись при ручном «стряхивании», обогащал популяцию митотических клеток.
Анализ клеточного цикла
Распределение фаз клеточного цикла определяли путем анализа содержания ДНК с помощью либо проточной цитометрии (BD FACS Canto™ II), либо проточной цитометрии с визуализацией. Клетки фиксировали в ледяном этаноле (70%), обрабатывали рибонуклеазой А (100 мкг/мл) и окрашивали йодидом пропидия (PI, 50 мкг/мл) или фиксировали в растворе А FIX&PERM ® (Nordic MUbio) и окрашивали DAPI (1 мкг/мл). Митотические клетки также идентифицировали с помощью проточной цитометрии с использованием антитела против фосфогистона h4 (Ser28). Лизаты клеток оценивали вестерн-блоттингом с использованием антитела против фосфогистона h4 (Ser10/Thr11) в качестве дополнительного митотического маркера. Морфологию хроматина и антифосфогистона h4 (Ser28) использовали для определения клеток в указанных фазах клеточного цикла и митоза в экспериментах по конфокальной микроскопии.
Эволюционный анализ
Чтобы установить эволюционную траекторию REAF, мы проанализировали выравнивание последовательностей ДНК REAF от 15 видов современных приматов, используя codeml (как реализовано PAML 4.2) (28). Эволюцию REAF сравнивали с несколькими моделями выбора NSsites, M1, M7 и M8a (нейтральные модели с классами сайтов dN/dS <1 или ≤1) и M2, M8 (модели положительного отбора, допускающие дополнительный класс сайтов с dN/ dS >1). В моделировании максимального правдоподобия использовались две модели частот кодонов (F61 и F3×4) и два разных начальных значения для dN/dS (ω). Были проведены тесты отношения правдоподобия, чтобы оценить, какой модели эволюции данные соответствуют значительно лучше. Значение р указывает на уверенность, с которой нулевая модель (М1, М7, М8а) может быть отвергнута в пользу модели положительного отбора (М2, М8). Выравнивание REAF было проанализировано с помощью GARD, чтобы подтвердить отсутствие рекомбинации во время эволюции REAF (29). Ни положительно отобранные сайты, ни сигнатуры эпизодического диверсифицирующего отбора не были обнаружены в REAF дополнительным эволюционным анализом с помощью REL и FEL или MEME (30).
Доступность данных
Все данные микрочипов доступны в сводной базе данных экспрессии генов (GEO) под номером доступа GSE54455.
Благодарности
Моноклональные антитела к p24 ВИЧ-1 (EVA365 и 366) были предоставлены Центром реагентов против СПИДа EVA программы ЕС, NIBSC, Великобритания (номер контракта AVIP LSHP-CT-2004-503487). Мы благодарим Paul Clapham, Robin Weiss и Ari Fasatti за критический обзор рукописи.
Ссылки
- 1.↵
Экштейн Д.А., Шерман М.П., Пенн М.Л., Чин П.С., Де Норонья С.М., Грин В.К., и др. Vpr ВИЧ-1 увеличивает вирусную нагрузку, способствуя инфицированию тканевых макрофагов, но не неделящихся CD4+ Т-клеток. J Exp Med . 2001;194(10):1407–19.
- 2.↵
Малим М.Х., Эмерман М. Дополнительные белки ВИЧ-1 – обеспечение выживания вируса во враждебной среде. Микроб-хозяин клетки . 2008;3(6):388–98.
- 3.
Коннор Р.И., Чен Б.
 К., Чоу С., Ландау Н.Р. Vpr необходим для эффективной репликации вируса иммунодефицита человека типа 1 в мононуклеарных фагоцитах. Вирусология . 1995;206(2):935–44.
К., Чоу С., Ландау Н.Р. Vpr необходим для эффективной репликации вируса иммунодефицита человека типа 1 в мононуклеарных фагоцитах. Вирусология . 1995;206(2):935–44. - 4.
Heinzinger NK, Bukrinsky MI, Haggerty SA, Ragland AM, Kewalramani V, Lee MA, et al. Белок Vpr вируса иммунодефицита человека типа 1 влияет на ядерную локализацию вирусных нуклеиновых кислот в неделящихся клетках-хозяевах. Proc Natl Acad Sci U S A . 1994;91(15):7311–5.
- 5.
Vodicka MA, Koepp DM, Silver PA, Emerman M. Vpr ВИЧ-1 взаимодействует с ядерным транспортным путем, способствуя заражению макрофагами. Гены Дев . 1998;12(2):175–85.
- 6.
Balliet JW, Kolson DL, Eiger G, Kim FM, McGann KA, Srinivasan A. Отличительные эффекты в первичных макрофагах и лимфоцитах дополнительных генов вируса иммунодефицита человека типа 1 vpr, vpu и nef: мутационные анализ первичного изолята ВИЧ-1. Вирусология .
 1994; 200.
1994; 200. - 7.↵
Chen R, Le Rouzic E, Kearney JA, Mansky LM, Benichou S. Vpr-опосредованное включение UNG2 в частицы ВИЧ-1 необходимо для модуляции скорости мутации вируса и репликации в макрофагах. J Биол Хим . 2004;279(27):28419–25.
- 8.↵
Коэн Э.А., Тервиллигер Э.Ф., Джалинус Ю., Пру Дж., Содроски Дж.Г., Хазелтин В.А. Идентификация продукта и функции vpr ВИЧ-1. J Приобретенный иммунодефицитный синдром . 1990;3(1):11–8.
- 9.↵
Бачанд Ф., Яо XJ, Хримеч М., Ружо Н., Коэн Э.А. Включение Vpr в вирус иммунодефицита человека типа 1 требует прямого взаимодействия с доменом p6 предшественника gag p55. J Биол Хим . 1999;274(13):9083–91.
- 10.↵
Marno KM, O’Sullivan E, Jones CE, Diaz-Delfin J, Pardieu C, Sloan RD, et al. РНК-ассоциированный противовирусный фактор ранней стадии является основным компонентом рестрикции Lv2. Дж Вирол .
 2017;91(10).
2017;91(10). - 11.↵
Desai TM, Marin M, Sood C, Shi J, Nawaz F, Aiken C, et al. Меченный флуоресцентным белком Vpr отделяется от ядра ВИЧ-1 после слияния с вирусом и быстро проникает в ядро клетки. Ретровирусология . 2015;12:88.
- 12.↵
Marno KM, Ogunkolade BW, Pade C, Oliveira NM, O’Sullivan E, McKnight A. Новый фактор рестрикции РНК-ассоциированный антивирусный фактор ранней стадии (REAF) ингибирует иммунодефицит человека и обезьян вирусы. Ретровирусология . 2014;11:3.
- 13.↵
Романи Б., Коэн Э.А. Дополнительные белки Vpr и Vpx лентивируса узурпируют убиквитинлигазу cullin4-DDB1 (DCAF1) E3. Карр Опин Вирол . 2012;2(6):755–63.
- 14.↵
Laguette N, Bregnard C, Hue P, Basbous J, Yatim A, Larroque M, et al. Преждевременная активация комплекса SLX4 с помощью Vpr способствует аресту G2/M и ускользанию от врожденного иммунного восприятия.
 Сотовый . 2014;156(1-2):134-45.
Сотовый . 2014;156(1-2):134-45. - 15.↵
Lahouassa H, Blondot ML, Chauveau L, Chougui G, Morel M, Leduc M, et al. Vpr ВИЧ-1 разрушает транслоказу ДНК HLTF в Т-клетках и макрофагах. Proc Natl Acad Sci U S A . 2016;113(19):5311–6.
- 16.↵
Марешал А., Ли Дж.М., Джи Сюй, Ву К.С., Язински С.А., Нгуен Х.Д. и др. PRP19 трансформируется в сенсор RPA-оцДНК после повреждения ДНК и управляет активацией ATR через убиквитин-опосредованную схему. Мол Ячейка . 2014;53(2):235–46.
- 17.↵
Хелмер Р.А., Мартинес-Загилан Р., Дертьен Дж.С., Фулфорд С., Форман О., Пейрис В. и др. Геликазоподобный транскрипционный фактор (Hltf) регулирует переход G2/M, кардиальные транскрипционные сети Wt1/Gata4/Hif-1a и биогенез коллагена. PLoS Один . 2013;8(11):e80461.
- 18.↵
Вэй Ю., Ю Л., Боуэн Дж., Горовский М.А., Эллис К.Д. Фосфорилирование гистона h4 необходимо для правильной конденсации и сегрегации хромосом.
 Сотовый . 1999;97(1):99–109.
Сотовый . 1999;97(1):99–109. - 19.↵
Groschel B, Bushman F. Остановка клеточного цикла в G2/M способствует ранним стадиям инфицирования вирусом иммунодефицита человека. Дж Вирол . 2005;79(9):5695–704.
- 20.↵
Balliet JW, Kolson DL, Eiger G, Kim FM, McGann KA, Srinivasan A, et al. Различные эффекты в первичных макрофагах и лимфоцитах дополнительных генов vpr, vpu и nef вируса иммунодефицита человека типа 1: мутационный анализ первичного изолята ВИЧ-1. Вирусология . 1994; 200(2):623–31.
- 21.↵
Дойл Т., Гужон С., Малим М.Х. ВИЧ-1 и интерфероны: кто кому мешает? Nat Rev Microbiol . 2015;13(7):403–13.
- 22.↵
Kluge SF, Sauter D, Kirchhoff F. SnapShot: противовирусные факторы рестрикции. Сотовый . 2015;163(3):774–e1.
- 23.↵
Гужон К., Малим М.Х. Характеристика постэнтерального блока, индуцированного альфа-интерфероном, к инфекции ВИЧ-1 в первичных макрофагах и Т-клетках человека.
 Дж Вирол . 2010;84(18):9254–66.
Дж Вирол . 2010;84(18):9254–66. - 24.↵
Чейни К.М., Макнайт А. Интерферон-альфа опосредует ограничение репликации вируса иммунодефицита человека типа 1 в первичных макрофагах человека на ранней стадии репликации. PLoS Один . 2010;5(10):e13521.
- 25.↵
McLaren PJ, Gawanbacht A, Pyndiah N, Krapp C, Hotter D, Kluge SF, et al. Идентификация потенциальных факторов ограничения ВИЧ путем объединения эволюционных геномных сигнатур с функциональным анализом. Ретровирусология . 2015;12:41.
- 26.↵
Мюррелл Б., Фоллбрехт Т., Гуателли Дж., Вертхейм Д.О. Эволюционная история антиретровирусных белков SERINC3 и SERINC5 не поддерживает эволюционную гонку вооружений у приматов. Дж Вирол . 2016;90(18):8085–9.
- 27.↵
Джеффри CJ. Введение в белковый совместный труд. Биохим Сок Транс . 2014;42(6):1679–83.
- 28.

Ян З. PAML 4: филогенетический анализ методом максимального правдоподобия. Мол Биол Эвол . 2007;24(8):1586–91.
- 29.
Косаковский пруд С.Л., Посада Д., Гравенор М.Б., Воелк С.Д., Фрост С.Д. GARD: генетический алгоритм обнаружения рекомбинации. Биоинформатика . 2006;22(24):3096–8.
- 30.
Pond SL, Frost SD. Datamonkey: быстрое обнаружение селективного давления на отдельные сайты выравнивания кодонов. Биоинформатика . 2005;21(10):2531–3.
Наверх
Программа Research Instrumentation Fund (RIF) — Вице-президент по исследованиям
Руководство программы на 23 финансовый год
Описание программы
Критерии приемлемости
Важные сроки
Требования программы
Требуемые материалы заявки
Процесс проверки и критерии подачи информации и итоговый отчет
Приложение
Контактная информация
Описание программы
Фонд исследовательского оборудования (RIF) оказывает поддержку преподавателям и основным учреждениям
для покупки нового оборудования или для замены/обновления существующего исследовательского оборудования. Оборудование
Оборудование
купленные на средства RIF, предназначены для максимально широкого использования и должны
используется для содействия исследованиям и стипендиям, финансируемым извне. Решения о финансировании
на основе достоинства предложения, продемонстрированной необходимости, влияния оборудования на
Исследовательское сообщество UofU и наличие средств.
Начиная с 23 финансового года программа RIF будет проводить один цикл программы RIF. РИФ
Программа стала экспоненциально более конкурентоспособной по мере расширения нашего исследовательского сообщества.
его объем и влияние. Реструктуризация программы для приема заявок один раз в год
предоставит заявителям значительное время для подготовки хорошо структурированного и высококонкурентного
Предложение РИФ. Если цикл 23 ФГ не использует весь программный бюджет, VPR
Office рассмотрит второй программный цикл после закрытия первого.
Если у вас есть срочный запрос на покупку, модернизацию или замену оборудования, которое
возникает до или после крайнего срока 23 ФГ, отправьте запрос по адресу [email protected]. Это только для срочных запросов. Запросы, которые не являются срочными, будут автоматически отклонены и
исследователю будет предложено представить следующий доступный цикл RIF.
Критерии приемлемости
Фонд исследовательского оборудования доступен для:
- Постоянные преподаватели и преподаватели карьерного роста, имеющие должность не менее 0,75 FTE
на момент подачи. Только одна заявка на одного заявителя. - Признано основным оборудованием Университета Юты. (Примечание. Запросы на основное оборудование могут инициировать только директора основных объектов. Только
один запрос на основное средство в каждом цикле. )
)
Важные сроки
Начиная с 23 финансового года программа RIF будет проводить один цикл программы RIF. Приложения
должны быть отправлены по номеру в среду, 11 января 2023 г., до 23:59 (МСК). Если цикл 23 ФГ не использует весь программный бюджет, Управление VPR рассмотрит
второй программный цикл после закрытия первого.
Требования программы
Сопутствующие средства: Сопутствующие средства необходимы для рассмотрения заявки на получение награды RIF. Соответствие
средства являются показателем поддержки со стороны кафедры/колледжа и/или оборудования абитуриента
пользователей и продемонстрировать важность приобретения для тех, кто поддерживает приложение.
Минимум 30% в соответствующих фондах требуется, за исключением хорошо документированных и исключительных случаев.
обстоятельства. В заявке должен быть указан источник соответствующих средств.
Непредоставление суммы и информации об источнике для всех соответствующих фондов может отрицательно сказаться на
влияют на приложение RIF. Обратите внимание, что 30% средств на совпадении — это только минимум.
количество. Запросы на большие суммы должны по возможности учитывать средства, превышающие 30%.
Заявки с общей суммой запросов VPR, превышающей 250 000 долларов США, вряд ли будут
финансируется без значимого обоснования и исключительно сильной демонстрации
поддерживать.
Документация по лучшей цене: Управление VPR настоятельно рекомендует преподавателям и активистам искать лучшую цену на оборудование,
и предоставить документацию об этих переговорах в качестве поддержки их применения.
Такие скидки будут учитываться при оценке заявки RIF. Производство
Производство
однако скидки и пожертвования в натуральной форме не считаются соответствующими фондами.
Инструменты для преподавания/обучения: средства RIF возникают за счет возмещения косвенных затрат.
из исследовательских контрактов и грантов, и, следовательно, предназначены исключительно для исследований и
не для целей обучения/обучения. По запросу также будет использоваться инструментарий
для обучения/обучения должна быть указана доля использования для обучения/обучения
и финансирование этой части приобретения, обслуживания и использования должно быть
идентифицировано. Соответствующие средства для целей обучения/обучения не зависят от
соответствующие средства для исследовательских целей.
Проверка оборудования: RIF предназначен для предоставления нового исследовательского оборудования ИЛИ для замены/модернизации существующих
исследовательские инструменты. Пожалуйста, убедитесь, что аналогичное оборудование в настоящее время недоступно
Пожалуйста, убедитесь, что аналогичное оборудование в настоящее время недоступно
в кампусе через поиск оборудования. Если имеется аналогичное оборудование, заявитель
необходимо предоставить обоснованное обоснование необходимости дополнительного оборудования.
Приложения RIF, не дающие обоснованного обоснования потребности в оборудовании, будут
не подлежат рассмотрению.
Запрещенное оборудование: Программа RIF не может финансировать компьютер или оборудование для сбора/хранения данных.
Из-за глобальной нехватки гелия UHP программа RIF на 23 финансовый год не может финансировать какие-либо
новое исследовательское оборудование, для работы которого требуется гелий UHP.
Запросы на замену оборудования: Запросы на замену оборудования должны содержать документацию о предыдущем использовании, например,
журнал, показывающий доход и базу пользователей.
Запросы на повторную отправку RIF: Повторно отправленные предложения должны включать пошаговый ответ всем предыдущим рецензентам.
комментарии, в которых четко указывается а) в чем заключались прежние опасения и б) как новые
предложение рассмотрело или разъяснило эти комментарии и опасения. Приложение будет
быть автоматически отклонено, если оно не отвечает адекватно предыдущим рецензентам
комментарии и опасения. Комментарии рецензента можно найти под исходной заявкой.
подача в InfoReady. Пожалуйста, свяжитесь с [email protected], если вы не можете найти свой
комментарии к предыдущему отзыву.
Необходимые материалы заявки
Материалы заявки принимаются через InfoReady. Может потребоваться загрузка некоторых документов.
Пожалуйста, загружайте все документы только в формате PDF или Excel.
1. Обзор заявителя/оборудования
- Информация о заявителе
- Наименование запрашиваемого оборудования
- Краткое описание/обзор оборудования
- Общая стоимость оборудования
- Соответствующие фонды Всего
- Соответствующий источник средств (включая выделенные доллары на каждый источник)
- Затраты на установку или обучение (должны быть указаны/обоснованы)
- Общая сумма, запрошенная по программе VPR RIF
Примечание. Заявки с общей суммой запроса VPR, превышающей 250 000 долларов США, маловероятны.
финансироваться без значимого обоснования и исключительно сильной демонстрации
поддержки.
2. Информация об оборудовании
- Проверка того, что оборудование является уникальным/новым для Университета, ИЛИ его замена или модернизация
к существующему оборудованию.
- Как оборудование будет управляться и обслуживаться (включая предполагаемый срок службы и
потребности в постоянном техническом обслуживании оборудования) - Ожидаемые ежегодные затраты на обслуживание и ремонт
- Как будут поддерживаться текущие/периодические расходы
- План предоставления доступа другим исследователям, в том числе из других отделов/колледжей
(сроки, система бронирования, стоимость/пополнение и т.д.) - Где будет размещено оборудование (Основные директора должны предоставить обоснование, если оборудование
не будет размещаться на основном объекте) - Кандидаты на факультеты должны предоставить письмо поддержки от основного директора, если размещают оборудование
на основном объекте - Влияние оборудования/награды RIF на стипендию и производительность (в результате оборудования)
- Воздействие оборудования/гранта RIF на получение внешнего финансирования (в результате оборудования)
3. Письма поддержки
Письма поддержки
Заявители должны указать
- (1) письмо поддержки от декана колледжа
- (1) письмо поддержки от заведующего кафедрой
- (1) письмо поддержки от КАЖДОГО источника финансирования
- (неограниченное количество) письма поддержки от дополнительных пользователей вспомогательного факультета
Примечание. Кандидаты, намеревающиеся разместить оборудование в основном учреждении, должны приложить письмо
от директора основного объекта с указанием поддержки оборудования и того, как
предприятие готово управлять/обслуживать оборудование от имени PI, и
как оборудование может повлиять на стратегические приоритеты объекта
4. Загрузка ценового предложения по оборудованию
- Все кандидаты должны загрузить ценовое предложение на запрашиваемое оборудование.
 Цитаты не могут быть
Цитаты не могут быть
старше трех месяцев.
5. Заявление о повторной подаче (если применимо)
- Все ЗАЯВЛЕНИЯ должны включать пошаговый ответ всем предыдущим рецензентам.
комментарии, в которых четко указывается, как новое предложение решает или разъясняет эти
комментарии и опасения. Это должно быть включено в «Заявление о повторной подаче».
поле загрузки в конкурсе InfoReady. Новые предложения не требуются для завершения
этот шаг.
Процесс рассмотрения и критерии оценки
Заявки RIF рассматриваются Комитетом по рассмотрению RIF. Ревизионный комитет РИФ
состоит из коллег заявителя, бывших получателей финансирования RIF и руководства университета.
Рекомендации по финансированию RIF представляются VPR.
Заявки на РИФ оцениваются по:
- Общая значимость и обоснованность заявки
- Влияние запрошенного оборудования на стипендию и исследовательскую продуктивность
- Сформулированная потребность в запрашиваемом оборудовании
- Соотношение затрат и выгод запрашиваемого оборудования
- Предлагаемый план размещения и предоставления общего доступа к оборудованию
- Качество плана управления/обслуживания оборудования (включая план текущих/периодических
расходы, связанные с оборудованием) - Предлагаемый план использования оборудования для продвижения/облегчения возможности внешнего финансирования
материалы факультета UofU - Поддержка со стороны декана, заведующего кафедрой и поддержки пользователей факультета
Информация об итоговом отчете
Получатель любого механизма внутреннего гранта VPR должен представить итоговый отчет
в течение 90 дней до истечения срока действия проекта, как указано в исходной награде.


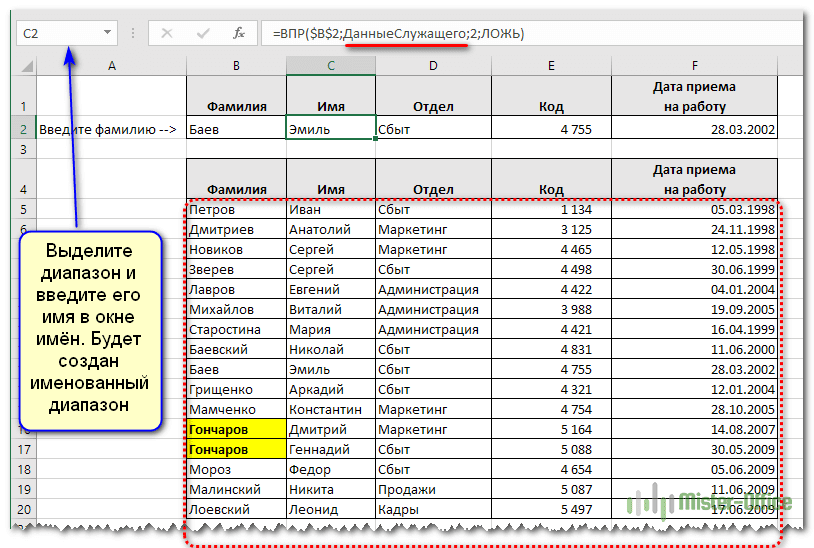
 Например, =ВПР(«Иванов»;A1:B100;2;ЛОЖЬ).
Например, =ВПР(«Иванов»;A1:B100;2;ЛОЖЬ).
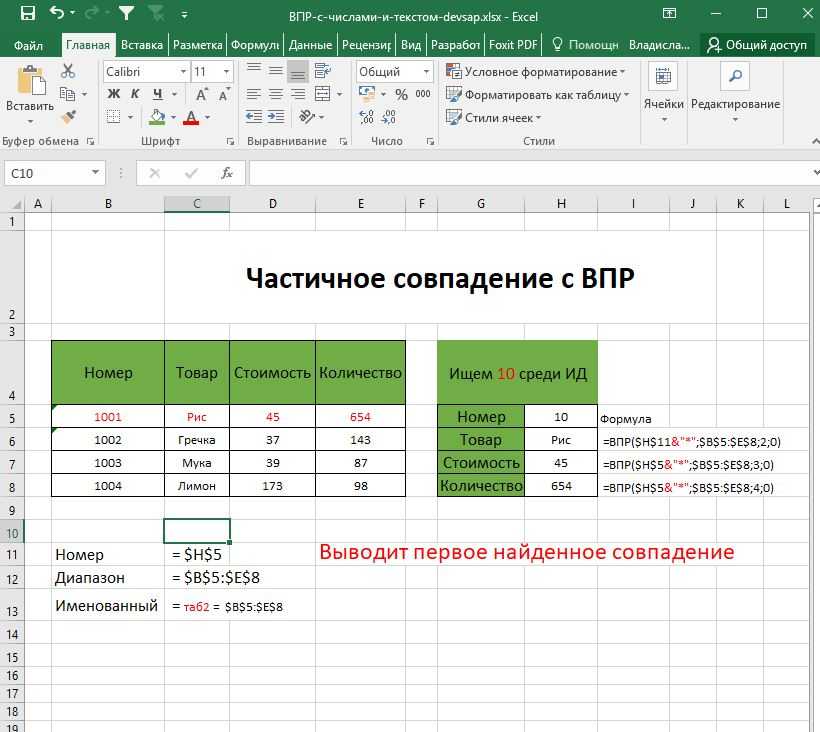

 Если первый столбец не отсортирован, возвращаемое значение может быть непредвиденным. Отсортируйте первый столбец или используйте значение ЛОЖЬ для точного соответствия.
Если первый столбец не отсортирован, возвращаемое значение может быть непредвиденным. Отсортируйте первый столбец или используйте значение ЛОЖЬ для точного соответствия.
 в статье Исправление ошибки #ЗНАЧ! в функции ВПР.
в статье Исправление ошибки #ЗНАЧ! в функции ВПР.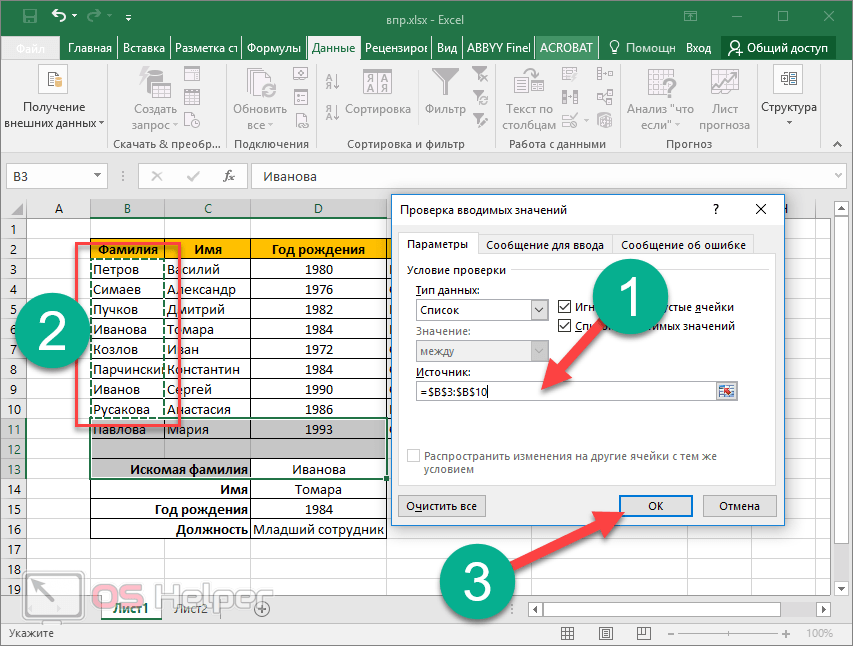 Кроме того, вы можете использовать традиционный метод ВПР и ссылаться на одну ячейку вместо целого столбца: =ВПР(A2;A:C;2;ЛОЖЬ).
Кроме того, вы можете использовать традиционный метод ВПР и ссылаться на одну ячейку вместо целого столбца: =ВПР(A2;A:C;2;ЛОЖЬ).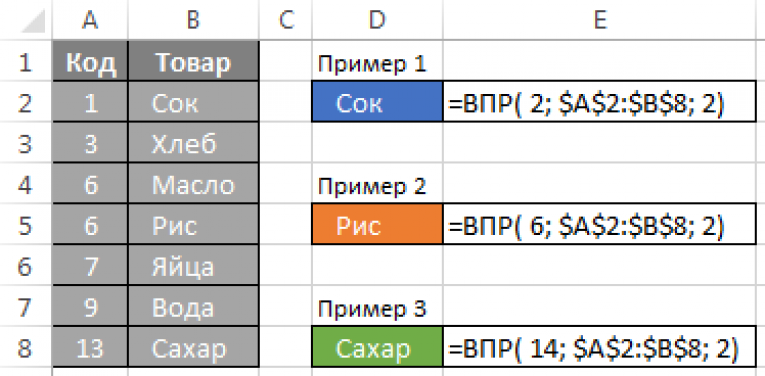
 Вопросительный знак соответствует любому отдельно взятому символу. Звездочка — любой последовательности символов. Если требуется найти именно вопросительный знак или звездочку, следует ввести значок тильды (~) перед искомым символом.
Вопросительный знак соответствует любому отдельно взятому символу. Звездочка — любой последовательности символов. Если требуется найти именно вопросительный знак или звездочку, следует ввести значок тильды (~) перед искомым символом.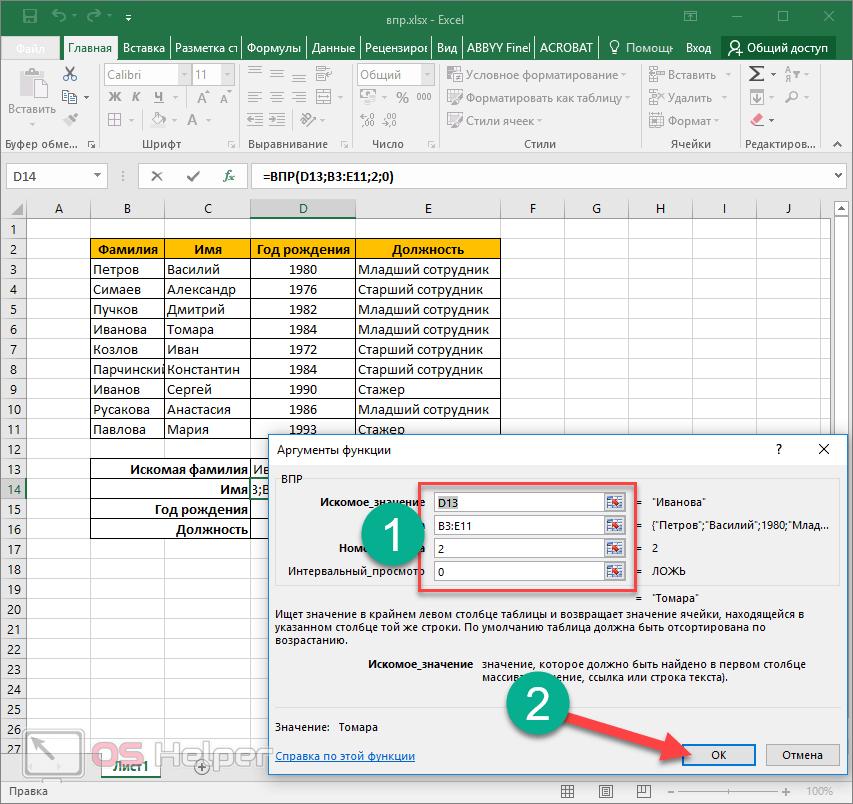
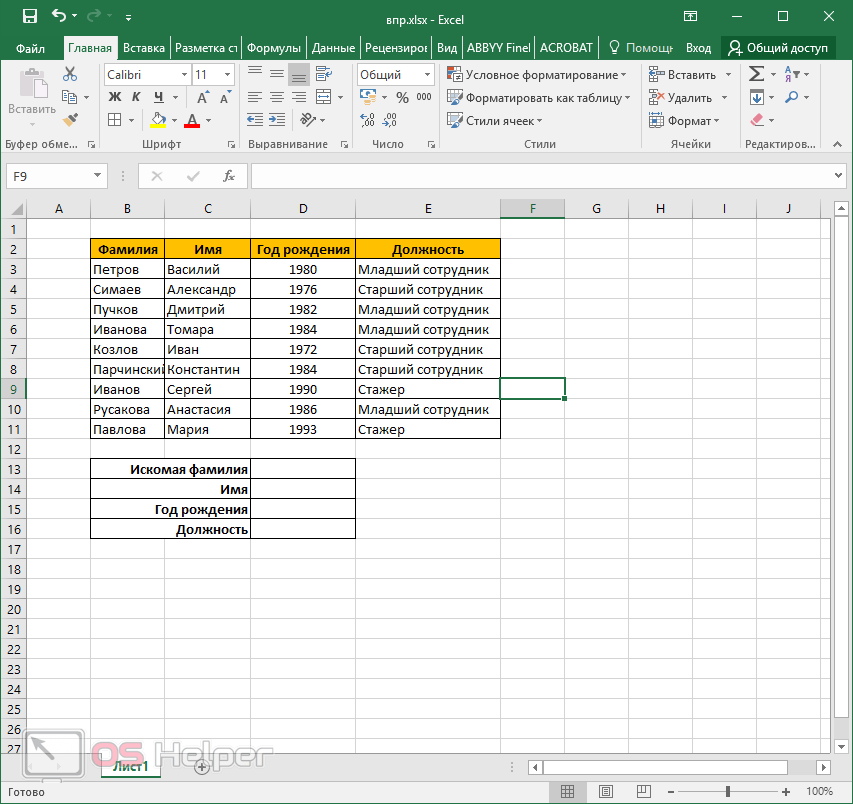
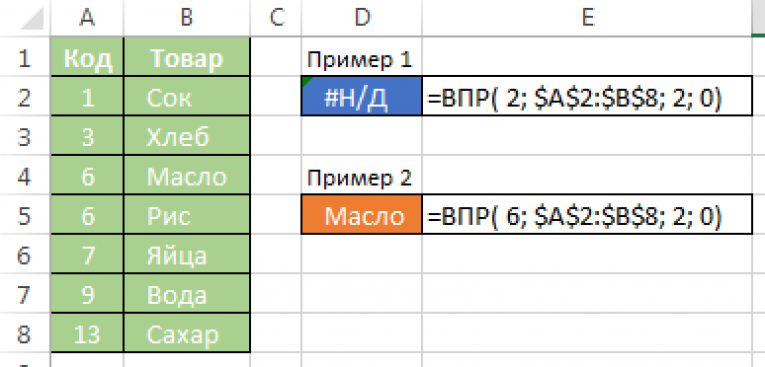 Затем взять данные из второго столбца нового прайса (новую цену) и подставить их в ячейку С2.
Затем взять данные из второго столбца нового прайса (новую цену) и подставить их в ячейку С2.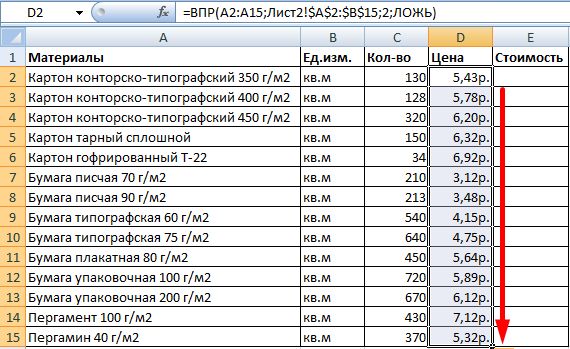 Excel находит нужную цену.
Excel находит нужную цену.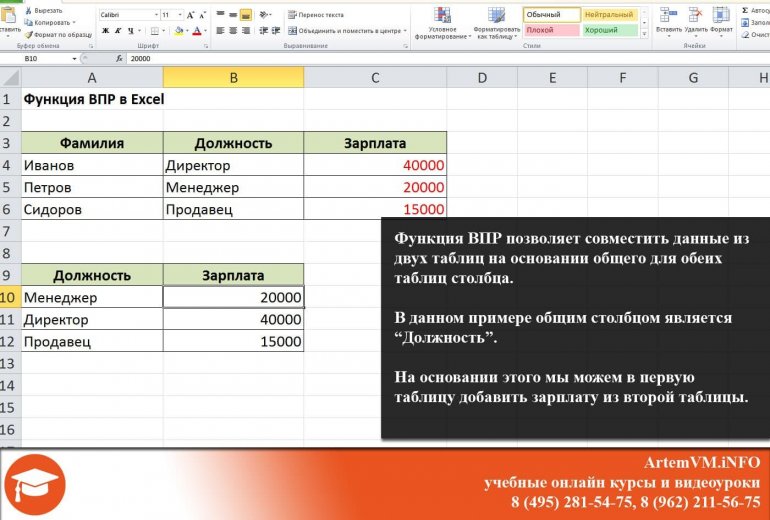 Таблица – диапазон с названиями материалов и ценами. Столбец, соответственно, 2. Функция приобрела следующий вид: .
Таблица – диапазон с названиями материалов и ценами. Столбец, соответственно, 2. Функция приобрела следующий вид: .